
题目列表(包括答案和解析)







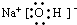
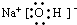
 H++HO2ˉ
H++HO2ˉ H++HO2ˉ
H++HO2ˉ| c2(SO3) |
| c(O2)?c2(SO2) |
| c2(SO3) |
| c(O2)?c2(SO2) |
A、B、C、D、E是原子序数依次增大的短周期元素,A、D在周期表中的相对位置如表,且元素A的最高正化合价与最低负化合价的绝对值相差2,B与D属于同主族元素;元素C是一种银白色金属,放置在空气中会迅速变暗。

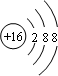
(1)D的原子结构示意图为 ;
(2)元素E在元素周期表中位于第 族;
(3)C、D、E离子半径的大小关系为 (用离子符号表示);
(4)元素B的单质与元素C的单质加热时生成化合物甲,化合物甲中所含化学键为
试写出甲与水反应的离子方程式 ;
(5)若乙是元素A的最简单气态氢化物,丙是元素C的最高价氧化物对应的水化物。
①pH相同的乙和丙的水溶液,分别用蒸馏水稀释到原来的x、y倍,稀释后两种溶液的pH仍然相同,则x y(填写“>”、“<”或“=” )
②在微电子工业中,乙的水溶液常用作刻蚀剂H2O2的清除剂,反应的产物不污染环境,其化学方程式为 (不需要配平)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com