
题目列表(包括答案和解析)
| ||
| ||

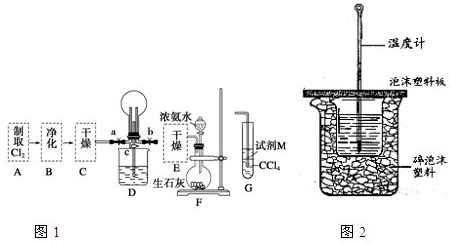
某化学实验小组欲制取氧化铜并证明氧化铜能加快氯酸钾的分解,进行了如下实验:
(I)制取氧化铜
(1)称取2gCuSO45H2O在________(填仪器)中研细后倒入烧杯,加10mL蒸馏水溶解。
(2)向上述CuSO4溶液中逐滴加入NaOH溶液,立即产生蓝色沉淀,继续滴加,直到不再产生沉淀。然后将所得混合物转移到________(填仪器)中,加热至沉淀全部变为黑色,停止加热。
(3)将步骤(2)所得混合物过滤、洗涤,晾干后研细备用。
回答下列问题:
①完成上面的空白。
②上述实验步骤中需要使用玻璃棒的是________(填实验序号)。
③步骤(3)中洗涤沉淀的操作是________
(Ⅱ)该小组同学从资料中得知氧化铜也能催化分解氯酸钾。他们为了比较氧化铜和氧化锰的催化效果,设计用右图装置进行实验,实验时均以生成25mL气体为准。其它可能影响实验的因素均已控制,相关数据见下表:


回答下列问题.
④上述实验中的待测数据指________
⑤若(5)(6)中待测数据分别为10和7(单位相同),则________(填写化学式)催化效果好。
⑥为探究CuO在实验(5)中是否起催化作用,需补做如下实验(无需写出具体操作):a________,b验证CuO的化学性质没有改变。
某化学实验兴趣小组在“探究氯水与溴化亚铁溶液反应”的实验中发现:“在足量的溴化亚铁溶液中,加入1~2滴氯水,振荡后溶液呈黄色。”
| 【资料】 | 溴水是溴单质的水溶液,因溶有溴单质而呈黄色。 |
根据已有化学知识及资料,请你参与上述现象形成原因的分析与探究:
(1)提出问题猜想:
溶液呈黄色是因发生离子反应① (填离子方程式)所致。
溶液呈黄色是因发生离子反应② (填离子方程式)所致。
(2)设计实验并验证
为验证①与②中是哪个原因导致了溶液变黄色,设计并进行了以下实验。请根据以下所给试剂,进行合理选用,完成实验方案1和方案2:
| 试剂 | 酚酞试液、CCl4、无水酒精、KSCN溶液 | ||
| 方案 | 操作步骤 | 实验现象 | 结论 |
| 1 | 取所述黄色溶液于试管中,滴加 并振荡 | 溶液变红色 | 反应 所致 |
| 2 | 取所述黄色溶液于试管中,滴加 并振荡 | ________ ________ |
(3)实验结论:以上实验不仅验证了溶液变黄的真实原因,同时证明了Fe2+的还原性比Br- (填“强”或“弱”)。
(4)实验反思
I. 根据上述实验推测,若在溴化亚铁溶液中滴入足量氯水,再加入CCl4并充分振荡后静止,产生的现象是 。
Ⅱ. 在100 mLFeBr2溶液中通入2.24 L Cl2(标准状况),溶液中有1/2的Br-被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com