
题目列表(包括答案和解析)


(12分)为《京都议定书》2012年第一承诺期到期后的温室气体减排问题,世界各国都做出了不同的努力。随着新能源的开发和利用,CH3OH这个物质逐渐进入人们的视野,越来越受到人们的关注。
(1)下图是由CO(g)+2H2(g)→CH3OH(g)进行过程中的能量变化曲线。曲线a表示不使用催化剂时反应的能量变化,曲线b表示。下列相关说法正确的是( )
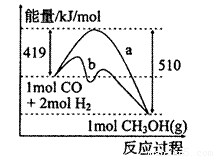
A.该反应是吸热反应
B.使用催化剂后反应热减小
C.热化学方程式为CO(g)+2H2(g) CH3OH(g) △H=-510kJ/mol
(2)由(1)推断,CO(g)+2H2(g)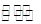 CH3OH(g)在密闭容器中进行,图中曲线a代表一定条件下该反应的过程。若使a曲线变为b曲线,可采取的措施是( )
CH3OH(g)在密闭容器中进行,图中曲线a代表一定条件下该反应的过程。若使a曲线变为b曲线,可采取的措施是( )
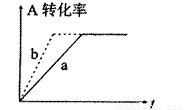
A.增大CO的浓度 B.缩小容器的容积
C.加入催化剂 D.升高温度
(3)由甲醇和氧气以及强碱做电解质溶液的新型燃料电池,正在逐步推广使用,假定放电过程中,甲醇完全氧化产生二氧化碳被充分吸收生成CO32-。该电池的负极反应的离子方程式为 ,放电过程中电池里溶液的pH将 (填“下降”、“上升”或“不变”);若有16克甲醇被完全氧化产生电能,并利用该过程中释放的电能电解足量的硫酸铜溶液,假设能量的利用率为80%。则得到氧气的物质的量是 。
(4)某同学将甲醇完全燃烧生成CO2气体通入200mL 0.1 mol/L的石灰水后,得到lg沉淀,那么通入的CO2的体积可能为(标态) 。

 CH3OH(g)在密闭容器中进行,图中曲线a代表一定条件下该反应的过程。若使a曲线变为b曲线,可采取的措施是( )
CH3OH(g)在密闭容器中进行,图中曲线a代表一定条件下该反应的过程。若使a曲线变为b曲线,可采取的措施是( )
(12分)为《京都议定书》2012年第一承诺期到期后的温室气体减排问题,世界各国都做出了不同的努力。随着新能源的开发和利用,CH3OH这个物质逐渐进入人们的视野,越来越受到人们的关注。
(1)下图是由CO(g)+2H2(g)→CH3OH(g)进行过程中的能量变化曲线。曲线a表示不使用催化剂时反应的能量变化,曲线b表示。下列相关说法正确的是( )
A.该反应是吸热反应
B.使用催化剂后反应热减小
C.热化学方程式为CO(g)+2H2(g) CH3OH(g) △H=-510kJ/mol
(2)由(1)推断,CO(g)+2H2(g)![]() CH3OH(g)在密闭容器中进行,图中曲线a代表一定条件下该反应的过程。若使a曲线变为b曲线,可采取的措施是( )
CH3OH(g)在密闭容器中进行,图中曲线a代表一定条件下该反应的过程。若使a曲线变为b曲线,可采取的措施是( )
A.增大CO的浓度 B.缩小容器的容积
C.加入催化剂 D.升高温度
(3)由甲醇和氧气以及强碱做电解质溶液的新型燃料电池,正在逐步推广使用,假定放电过程中,甲醇完全氧化产生二氧化碳被充分吸收生成CO32-。该电池的负极反应的离子方程式为 ,放电过程中电池里溶液的pH将 (填“下降”、“上升”或“不变”);若有16克甲醇被完全氧化产生电能,并利用该过程中释放的电能电解足量的硫酸铜溶液,假设能量的利用率为80%。则得到氧气的物质的量是 。
(4)某同学将甲醇完全燃烧生成CO2气体通入200mL 0.1 mol/L的石灰水后,得到lg沉淀,那么通入的CO2的体积可能为(标态) 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com