
题目列表(包括答案和解析)
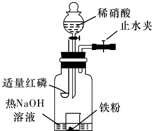 某同学用图示装置进行铁和稀硝酸反应的实验并进行相关的实验探究.
某同学用图示装置进行铁和稀硝酸反应的实验并进行相关的实验探究.(14分)某同学用图示装置进行铁和稀硝酸反应的实验并进行相关的实验探究。
a.向广口瓶内注入足量热NaOH溶液,将盛有一定质量的纯铁粉的小烧杯放入瓶中。
b.关闭止水夹,点燃红磷,伸人瓶中,塞好胶塞。
c.待红磷充分燃烧,一段时间后打开分液漏斗旋塞,向烧杯中缓慢滴入一定量的4mol·L-1的稀硝酸,
铁粉完全溶解。
(一)气体产物成分探究
(1)实验前如何检查该装置的气密性? 。
(2)燃烧红磷的目的是 。
(3)为证明气体产物为NO,步骤c后还缺少的一步主要操作是 。
(二)产物中铁元素价态探究:
(1)提出合理假设:
假设1:产物中只有+2价铁;假设2: ,假设3:产物中既有+2价铁,又有+3价铁。
(2)设计实验方案,验证假设1成立(写出实验操作步骤、现象和结论): 。
(三)问题讨论
(1)广口瓶中热NaOH溶液的主要作用是 。
(2)若假设3成立,且所得溶液中n(Fe2+):n(Fe3+)=3:1时,则对应的离子反应方程式为 。
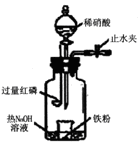

(16分)某同学用图示装置进行铁和稀硝酸反应的实验并进行相关的实验探究。(相对原子质量Fe:56)
a.向广口瓶内注入足量热NaOH溶液,将盛有a g纯铁粉的小烧杯放入瓶中。
b.关闭止水夹,点燃红磷,伸入瓶中,塞好胶塞。
c.待红磷充分燃烧,一段时间后打开分液漏斗旋塞,向烧杯中滴入200mL 6mol/L的稀硝酸,铁粉恰好完全溶解。
(一)气体产物成分探究
①实验前如何检查该装置的气密性 。
②燃烧红磷的目的是 。
③为证明气体产物为NO,步骤c后还缺少的一步主要操作是___________________。
(二)产物中铁元素价态探究:
(1)提出合理假设:
假设1:产物只有+3价铁;
假设2: ;
假设3: 。
(2)设计实验:分别取小烧杯中反应后溶液装入两支试管甲、乙,在甲试管中滴加酸性高锰酸钾溶液;在乙试管中滴加KSCN溶液,观察现象。推测实验现象与结论:
①若现象为: ,则假设1正确;
②若现象为: ,则假设2正确;
③若现象为: ,则假设3正确。
(3)a值范围为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com