
题目列表(包括答案和解析)
| A.烧杯中有铜无铁 | B.烧杯中有铁无铜 |
| C.烧杯中铁、铜都有 | D.烧杯中铁、铜都无 |
印制电路板时常用氯化铁溶液作为“腐蚀液”,发生的反应为:2FeCl3+Cu=2FeCl2+CuCl2,向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是??? (? )
? A.烧杯中有铜无铁?? B.烧杯中有铁无铜
? C.烧杯中铁、铜都有??? D.烧杯中铁、铜都无
印制电路板时常用氯化铁溶液作为“腐蚀液”,发生的反应为:
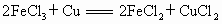 ,向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是
,向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是
[
]|
A .烧杯中有铜无铁 |
B .烧杯中有铁无铜 |
|
C .烧杯中铁、铜都有 |
D .烧杯中铁、铜都无 |
印制电路板时常用氯化铁溶液作为“腐蚀液”,发生的反应为:
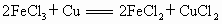 ,向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是
,向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是
[
]|
A .烧杯中有铜无铁 |
B .烧杯中有铁无铜 |
|
C .烧杯中铁、铜都有 |
D .烧杯中铁、铜都无 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com