
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
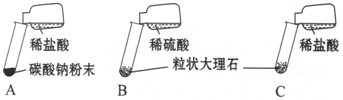
| ЪЕбщ | ЪЕбщЯжЯѓ | ЪЕбщФкШн |
| A | ОчСвЗДгІЃЌбИЫйЗХГіДѓСПЦјХн | ЗДгІЫйТЪЙ§ПьЃЌЦјЬхВЛБуЪеМЏЃЌВЛвЫгкЪЕбщЪвжЦШЁЖўбѕЛЏЬМ |
| B | ВњЩњЦјХнЃЌЫйТЪбИЫйМѕТ§ЃЌЗДгІМИКѕЭЃжЙ | ЮоЗЈГжајВњЩњCO2ЃЌВЛФмгУгкЪЕбщЪвжЦШЁCO2 |
| C | Ђй ВњЩњЦјХнЃЌЫйТЪЪЪжаЧвГжОУ ВњЩњЦјХнЃЌЫйТЪЪЪжаЧвГжОУ |
Ђк ФмГжајВњЩњCO2ЃЌЪЪгУгкЪЕбщЪвжЦШЁCO2 ФмГжајВњЩњCO2ЃЌЪЪгУгкЪЕбщЪвжЦШЁCO2 |
 ФГЪЕбщаЁзщЕФЭЌбЇгУЬМЫсФЦЗлФЉЁЂПХСЃзДДѓРэЪЏЁЂЯЁбЮЫсЁЂХЈбЮЫсЁЂЯЁСђЫсетМИжжвЉЦЗЃЌЬНОПЪЕбщЪвжЦШЁCO2ЕФЗДгІдРэЃЎЧыФуВЮгыЯТСаЬНОПВЂЛиД№ЮЪЬтЃЎ
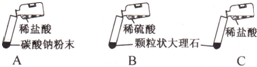
ФГЪЕбщаЁзщЕФЭЌбЇгУЬМЫсФЦЗлФЉЁЂПХСЃзДДѓРэЪЏЁЂЯЁбЮЫсЁЂХЈбЮЫсЁЂЯЁСђЫсетМИжжвЉЦЗЃЌЬНОПЪЕбщЪвжЦШЁCO2ЕФЗДгІдРэЃЎЧыФуВЮгыЯТСаЬНОПВЂЛиД№ЮЪЬтЃЎ| ЪЕбщ | ЪЕбщЯжЯѓ | ЕУГіЕФНсТл |
| A | ОчСвЗДгІЃЌбИЫйЗХГіДѓСПЦјХн | ЗДгІЫйТЪЙ§ПьЃЌЦјЬхВЛБуЪеМЏЃЌВЛвЫгкЪЕбщЪвжЦШЁCO2 |
| B | ВњЩњЦјХнЃЌЫйТЪбИЫйМѕТ§ЃЌЗДгІМИКѕЭЃжЙ | ЮоЗЈГжајВњЩњCO2ЃЌВЛФмгУгкЪЕбщЪвжЦШЁCO2 |
| C | ВњЩњДѓСПЦјХнЃЌЗДгІСЌајЧвГжајЪБМфНЯГЄ ВњЩњДѓСПЦјХнЃЌЗДгІСЌајЧвГжајЪБМфНЯГЄ |
ЗДгІЫйТЪЪЪжаЃЌЦјЬхБугкЪеМЏ ЗДгІЫйТЪЪЪжаЃЌЦјЬхБугкЪеМЏ |
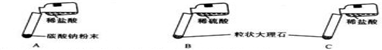
| ЪЕбщ | ЪЕбщЯжЯѓ | ЪЕбщФкШн |
| A | ОчСвЗДгІЃЌбИЫйЗХГіДѓСПЦјХн | ЗДгІЫйТЪЙ§ПьЃЌЦјЬхВЛБуЪеМЏЃЌВЛвЫгкЪЕбщЪвжЦШЁЖўбѕЛЏЬМ |
| B | ВњЩњЦјХнЃЌЫйТЪбИЫйМѕТ§ЃЌЗДгІМИКѕЭЃжЙЃЎ | ЮоЗЈГжајВњЩњCO2ЃЌВЛФмгУгкЪЕбщЪвжЦШЁCO2 |
| C | Ђй ВњЩњДѓСПЦјХн ВњЩњДѓСПЦјХн |
Ђк ЗДгІЫйТЪЪЪжаЃЌЦјЬхБугкЪеМЏ ЗДгІЫйТЪЪЪжаЃЌЦјЬхБугкЪеМЏ |
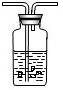
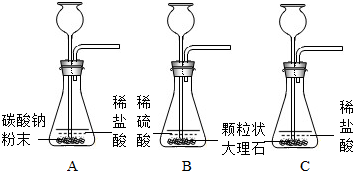
| ЪЕбщ | ЪЕбщЯжЯѓ | ЪЕбщНсТл |
| A | ОчСвЗДгІЃЌбИЫйЗХГіДѓСПЦјЬх | ЗДгІЫйЖШЙ§ПьЃЌЦјЬхВЛБуЪеМЏЃЌВЛвЫгУгкЪЕбщЪвжЦШЁCO2 |
| B | ВњЩњЦјХнЃЌЫйЖШбИЫйМѕТ§ЃЌМИУыжгКѓЗДгІМИКѕЭЃжЙ | ЮоЗЈГжајВњЩњЦјЬхЃЌВЛФмгУгкЪЕбщЪвжЦШЁCO2 |
| C | ______ | ______ |
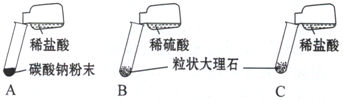
| ЪЕбщ | ЪЕбщЯжЯѓ | ЪЕбщФкШн |
| A | ОчСвЗДгІЃЌбИЫйЗХГіДѓСПЦјХн | ЗДгІЫйТЪЙ§ПьЃЌЦјЬхВЛБуЪеМЏЃЌВЛвЫгкЪЕбщЪвжЦШЁЖўбѕЛЏЬМ |
| B | ВњЩњЦјХнЃЌЫйТЪбИЫйМѕТ§ЃЌЗДгІМИКѕЭЃжЙ | ЮоЗЈГжајВњЩњCO2ЃЌВЛФмгУгкЪЕбщЪвжЦШЁCO2 |
| C | Ђй______ | Ђк______ |
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com