
题目列表(包括答案和解析)
某研究性学习小组设计了如下二组实验:
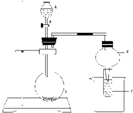
(I)实验验证元素周期律中, 非金属元素的非金属性越强,对应的最高价含氧酸的酸性就越强。设计了如下图装置以验证氮、碳、硅元素的非金属性强弱。
设计的实验可直接证明三种酸的酸性强弱,已知A是强酸,常温下可与铜反应;B是块状固体;打开分液漏斗的活塞后,C中可观察到有白色沉淀生成。
(1)写出所选用物质的化学式:
A: ,B: ,C: 。
(2)写出烧杯中发生反应的离子方程式: 。
(Ⅱ )为比较Fe3+和Cu2+对H2O2的催化效果,甲、乙两位同学分别设计了如图一、图二所示的实验。
(1)图一可通过观察
定性比较得出结论。有同学提出将CuSO4改为CuCl2更为合理,其理由是 ,或者将FeCl3溶液改成物质的量浓度为 mol/L的Fe2(SO4)3溶液。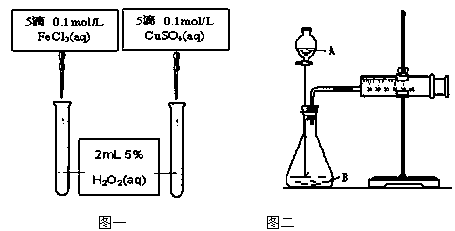
(2)检查图二装置气密性的方法是 ;
图二所示实验中需测量的数据是 。
某研究性学习小组设计了如下二组实验:
(I)实验验证元素周期律中, 非金属元素的非金属性越强,对应的最高价含氧酸的酸性就越强。设计了如下图装置以验证氮、碳、硅元素的非金属性强弱。

设计的实验可直接证明三种酸的酸性强弱,已知A是强酸,常温下可与铜反应;B是块状固体;打开分液漏斗的活塞后,C中可观察到有白色沉淀生成。
(1)写出所选用物质的化学式:
A: ,B: ,C: 。
(2)写出烧杯中发生反应的离子方程式: 。
(Ⅱ )为比较Fe3+和Cu2+对H2O2的催化效果,甲、乙两位同学分别设计了如图一、图二所示的实验。
(1)图一可通过观察
定性比较得出结论。有同学提出将CuSO4改为CuCl2更为合理,其理由是 ,或者将FeCl3 溶液改成物质的量浓度为 mol/L 的Fe2(SO4)3溶液。

(2)检查图二装置气密性的方法是 ;
图二所示实验中需测量的数据是 。
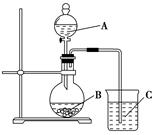
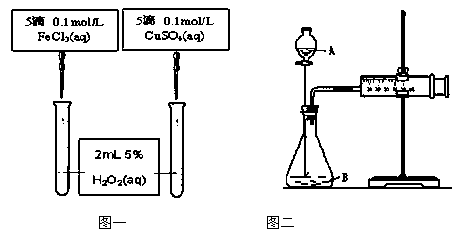
某校研究性学习小组设计了如下图所示装置进行下列有关实验.实验时将分液漏斗中A逐滴加入烧瓶中(图中铁架台、铁夹已略去).
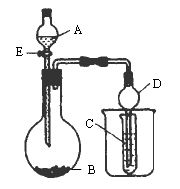
(1)若A为浓硫酸,B为第三周期元素组成的片状单质,其在常温下难与水反应,C为品红溶液,实验中观察到溶液红色褪去,则B为________(填化学式);然后向烧杯中加入沸水,又可观察到的现象是________.
(2)若B为块状大理石,C为Na2CO3饱和溶液,实验中观察到小试管内溶液变浑浊,则酸A不适宜用下列的________.
A.HCl
B.HNO3
C.H2SO4
(3)若B为生石灰,实验中观察到C溶液中生成白色沉淀,该沉淀既能溶于NaOH溶液,又能溶于稀盐酸,则A是________(填化学名称),C中生成的沉淀是________(填化学式)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com