
题目列表(包括答案和解析)
某短周期元素的原子最外层电子数为次外层的2倍,其单质甲可发生如下反应:
甲+乙(1)若丙为NO2.
①甲与乙反应的化学方程式为________.
②NO2可作火箭重要燃料-肼(N2H4)的助燃剂.已知:
N2(g)+2O2(g)=2NO2(g) ΔH=+67.7 kJ·mol-1,
2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g) ΔH=-1135.7 kJ·mol-1.
写出燃料-肼(N2H4)燃烧生成氮气和水蒸气的热化学方程式:________.
(2)若丙为SO2.
①把乙滴入硫酸铜晶体,观察到的现象是________.
②SO2能使酸性KMnO4溶液紫红色褪去,完成下列离子方程式:
③SO2在一定条件下,发生:2SO2(g)+O2(g)![]() 2SO3(g) ΔH<0反应.该反应的化学平衡常数K=________(填表达式);反应达平衡时,若改变其中一个条件x,则符合图中曲线的是________(填序号).
2SO3(g) ΔH<0反应.该反应的化学平衡常数K=________(填表达式);反应达平衡时,若改变其中一个条件x,则符合图中曲线的是________(填序号).
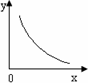
a.x表示温度,y表示SO2的物质的量
b.x表示压强,y表示SO2的转化率
c.x表示SO2的物质的量,y表示O2的物质的量
d.x表示SO3的物质的量,y表示化学平衡常数K
完成下列离子方程式
(1)BaCO3+( )=( )+CO2↑+H2O
(2)( )+( )=Cu(OH)2↓
(3)CO2+( )=![]() +H2O
+H2O
归纳整理是科学学习的重要方法之一。在学习了氧族元素的各种性质后,可归纳整理出如下所示的表格(部分)。
性质\元素 | 8O | 16S | 34Se | 52Te |
单质熔点(℃) | -218.4 | 113 | 450 | |
单质沸点(℃) | -183 | 444.6 | 685 | 1390 |
主要化合价 | -2 | -2,+4,+6 | -2,+4,+6 | |
原子半径 | 逐渐增大 | |||
单质与H2反应情况 | 点燃时易化合 | 加热化合 | 加热难化合 | 不能直接化合 |
请根据上表回答下列问题:
(1)硒的熔点范围可能是_________
(2)碲的化合价可能有_________
(3)硫、硒,碲的氢化物水溶液的酸性由强至弱的顺序是_________ (填化学式)。
(4)氢硒酸有较强的_________(填“氧化性”或“还原性”),因此放在空气中长期保存易变质,其可能发生的化学方程式为_________________________________。
(5)工业上Al2Te3可用来制备H2Te,完成下列化学方程式:
A12Te3 + ( ) A1(OH)3↓ + H2Te↑
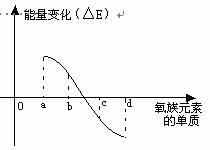
(6)右图所示为氧族元素单质与H2反应过程中的能量变化示意图,其中a、b、c、d分别表示氧族中某一元素的单质,△E为相同物质的量的单质与H2反应过程中的能量变化(反应的热效应)。则:b代表 ,d代表 (均写单质名称)。
(1)已知氢氧化铁可以被次氯酸钠氧化成![]() ,当3.21 g Fe(OH)3参加反应时,反应中共转移了0.09 mol电子,则n=________.
,当3.21 g Fe(OH)3参加反应时,反应中共转移了0.09 mol电子,则n=________.
(2)根据上题推断结果,配平下列离子方程式:
[ ]Fe(OH)3+[ ]ClO-+[ ]OH-——[ ]FeO4n-+[ ]Cl-+[ ]H2O
(3)结合以上反应,推测FeO4n-能与下列哪些物质反应(填序号)________.
A.Cl2
B.SO2
C.H2S
D.O2
已知Be、Al及其化合物性质相似。试完成下列化学方程式:
(1)Be(OH)2+H2SO4________。
(2)Be(OH)2+NaOH________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com