
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
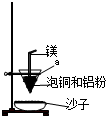 ЙЄвЕЩЯвБСЖБљЭЃЈmCu2O?nFeSЃЉПЩЕУЕНДжЭЃЌдйвдДжЭЮЊдСЯжЦБИСђЫсЭОЇЬхЃЎ
ЙЄвЕЩЯвБСЖБљЭЃЈmCu2O?nFeSЃЉПЩЕУЕНДжЭЃЌдйвдДжЭЮЊдСЯжЦБИСђЫсЭОЇЬхЃЎ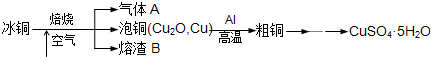
| ||
| ||
| ЕЮЖЈМС |
| 5bc |
| 4a |
| 5bc |
| 4a |
(1)ЕквЛДЮзі ЕФГЦСПЃЛЕкЖўДЮзі ЕФГЦСПЃЛЕкШ§ДЮзі ЕФГЦСПЃЛЕкЫФДЮзі ЕФГЦСПЁЃ
(2)ЕквЛЁЂЖўДЮГЦСПЕФФПЕФЪЧ ЃЌЕкШ§ЁЂЫФДЮГЦСПЕФФПЕФЪЧ ЁЃ
(3)ДгЯТСавЧЦїжабЁГіЪЕбщЫљашвЧЦї(гУзжФИЬюаД) ЃЌЛЙашвЊЕФвЧЦїЪЧ ЁЃ
A.ЭаХЬЬьЦН B.баВЇ C.ЪдЙмМа
D.ОЦОЋЕЦ E.еєЗЂУѓ F.ВЃСЇАє
G.лслі H.ИЩдяЦї I.ЪЏУоЭј
J.Ш§НХМм
(4)ЯТСаЧщПіЖдЪЕбщНсЙћдьГЩЕФЮѓВюЪЧЦЋИпЁЂЦЋЕЭЛЙЪЧВЛгАЯьЃП
a.дкПеЦјжаРфШД ( )
b.лсліВЛИЩдя ( )
c.лсліВЛНрОЛЃЌИНгаВЛЗжНтЕФЮлЮя ( )
d.СђЫсЭОЇЬхКЌгаВЛЗжНтЕФдгжЪ ( )
(5)ШєлсліЕФжЪСПЮЊm
ИљОнСђЫсЭОЇЬхНсОЇЫЎКЌСПЕФВтЖЈЪЕбщЃКЬюаДЯТСаПеАз
ДЫЪЕбщВйзїЫГађШчЯТЃКЂйГЦСПлсліЁЂОЇЬхЃЛЂкМгШШЁЂРфШДЃЛЂлГЦСПЃЛЂмдйМгШШЁЂРфШДЃЛЂнГЦСПЃЛЂоМЦЫуЃЛЂпЗжЮіЪЕбщЮѓВюЁЃ
ЃЈ1ЃЉгУЭаХЬЬьЦНГЦСПЕФЪБКђЃЌШєжИеыЦЋЯђзѓБпЃЌдђБэЪОЃЈЬюаДе§ШЗЕФбЁЯюДњТыЃЉ ЁЃ
AЃЎзѓХЬжиЃЌбљЦЗЧс BЃЎзѓХЬЧсЃЌэРТыжи
CЃЎгвХЬжиЃЌэРТыЧс DЃЎгвХЬЧсЃЌбљЦЗжи
ЃЈ2ЃЉдкНјааМгШШЪБЃЌгІИУгУ РДМаГжлсліЃЛЮЊСЫЗРжЙСђЫсЭОЇЬхЪЇШЅНсОЇЫЎЪБВЛЭъШЋЃЌЛђЗЂЩњCuSO4ЧПШШЗжНтЃЌдьГЩЪЕбщВњЩњЮѓВюЃЌЫљвддкМгШШВйзїжавЊЂй
Ђк ЁЃ
ЃЈ3ЃЉМгШШКѓЕФлслігІЗХдк жаРфШДЁЃШчЙћЗХдкПеЦјжаздШЛРфШДЃЌдђЛсЪЙЪЕбщНсЙћЕФЮѓВюЦЋ ЁЃ
ЃЈ4ЃЉдкНјааЂмЁЂЂнСНВНЪЕбщжаЃЌгаЪБЛЙвЊжиИДНјааЃЌетЪЧгЩгк ЁЃ
ЃЈ5ЃЉдкСђЫсЭОЇЬхНсОЇЫЎКЌСПЕФВтЖЈЪЕбщжаЃЌШєлсліЕФжЪСПЮЊmЃЌлслігыСђЫсЭОЇЬхЕФжЪСПЮЊm1ЃЌМгШШКѓГЦСПлслігыЮоЫЎСђЫсЭЕФжЪСПЮЊm2ЃЌдђОЇЬхжаНсОЇЫЎЕФжЪСПЗжЪ§Іи= ЃЈаДМЦЫуЪНЃЉЁЃШчЙћЪЕбщжаМгШШЮТЖШЙ§ИпЃЌЙЬЬхбеЩЋБфКкЃЌдђВтЖЈНсЙћЛс ЃЈЬюЁАВЛБфЁБЁЂЁАЦЋИпЁБЁЂЁАЦЋЕЭЁБЃЉЁЃ
вдЯТЪЧФГЭЌбЇВтЖЈСђЫсЭОЇЬхЃЈCuSO4ЁЄxH2OЃЉжаНсОЇЫЎКЌСПЕФЪЕбщЗНАИЁЃ
ЪЕбщгУЦЗЃКСђЫсЭОЇЬхЁЂбаВЇЁЂИЩдяЦїЁЂлсліЁЂШ§НХМмЁЂВЃСЇАєЁЂвЉГзЁЂЭаХЬЬьЦН
ЪЕбщВНжшЃК
Ђй зМШЗГЦСПвЛИіИЩОЛЁЂИЩдяЕФлсліЃЛ
Ђк дклсліжаМгШывЛЖЈСПЕФСђЫсЭОЇЬхЪдбљЃЌГЦжиЃЌНЋГЦСПЕФЪдбљЗХШыбаВЇжабаЯИЃЌдйЗХЛиЕНлсліжаЃЛ
Ђл НЋЪЂгаЪдбљЕФлсліМгШШЃЌД§ОЇЬхБфГЩАзЩЋЗлФЉЪБЃЌЭЃжЙМгШШЃЛ
Ђм НЋВНжшЂлжаЕФлсліЗХШыИЩдяЦїЃЌРфШДжСЪвЮТКѓЃЌГЦжиЃЛ
Ђн НЋВНжшЂмжаЕФлслідйМгШШвЛЖЈЪБМфЃЌЗХШыИЩдяЦїжаРфШДжСЪвЮТКѓГЦСПЁЃжиИДБОВйзїЃЌжБжССЌајСНДЮГЦСПЕФжЪСПВюВЛГЌЙ§0.1gЮЊжЙЃЛ
Ђо МЦЫуСђЫсЭОЇЬхЛЏбЇЪНжаxЕФЪЕбщжЕЁЃ
ЗжЮіИУЗНАИВЂЛиД№ЯТУцЮЪЬтЃК
ЃЈ1ЃЉЭъГЩБОЪЕбщЛЙашвЊЕФЪЕбщгУЦЗЪЧ ЃЛ
ЃЈ2ЃЉ жИГіЪЕбщВНжшЂкжаДцдкЕФДэЮѓВЂИФе§ЃК ЃЛ
ЃЈ3ЃЉСђЫсЭВЛФмЗХжУдкПеЦјжаРфШДЕФдвђЪЧ ЃЛ
ЃЈ4ЃЉВНжшЂнЕФФПЕФЪЧ ЃЛ
ЃЈ5ЃЉШєлсліЕФжЪСПЮЊmЃЌлслігыСђЫсЭОЇЬхЕФжЪСПЮЊm1ЃЌМгШШКѓГЦСПлслігыЮоЫЎСђЫсЭЕФжЪСПЮЊm2ЃЌдђОЇЬхCuSO4ЁЄxH2OжаЃЌx ЃН ЃЈаДБэДяЪНЃЉЃЛ
ЃЈ6ЃЉЯТУцЕФЧщПігаПЩФмдьГЩВтЪдНсЙћЦЋИпЕФЪЧ ЃЈЬюађКХЃЉЁЃ
AЃЎЪдбљжаКЌгаМгШШВЛЛгЗЂЕФдгжЪ BЃЎЪдбљжаКЌгаМгШШвзЛгЗЂЕФдгжЪ
CЃЎВтЪдЧАЪдбљвбгаВПЗжЭбЫЎ DЃЎЪЕбщЧАлсліЮДЭъШЋИЩдя
EЃЎОЇЬхМгШШЭбЫЎВЛЭъШЋ FЃЎМгШШЪБгаОЇЬхНІГі
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com