
题目列表(包括答案和解析)
请从给出的3道化学题中任选一题做答
1.[化学——选修化学与技术]
请回答氯碱工业中的如下问题:
(1)氯气、烧碱是电解食盐水时按照固定的比率k(质量比)生成的产品。理论上k__________(要求计算表达式和结果);
(2)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、 等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)、③BaCl2,这3种试剂添加的合理顺序是_________(填序号);
等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)、③BaCl2,这3种试剂添加的合理顺序是_________(填序号);
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。

①图中X、Y分别是_________、_________(填化学式),分析比较图示中氢氧化钠质量分数a%与b%的大小_________;
②分别写出燃料电池B中正极、负极上发生的电极反应
正极:_________;负极:_________;
③这样设计的主要节(电)能之处在于(写出2处)
___________________________、___________________________。
2.[化学——选修物质结构与性质]
已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子。X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子。请回答下列问题:
(1)X元素原子基态时的电子排布式为_________,该元素的符号为_________;
(2)Y元素原子的价层电子的轨道表示式为_________,该元素的名称是_________;
(3)X与Z可形成化合物XZ3,该化合物的空间构型为________________________;
(4)已知化合物X2Y3在稀硫酸溶液中可被金属锌还原为XZ3,产物还有ZnSO4和H2O,该反应的化学方程式是____________________________________;
(5)比较X的氢化物与同族第二、三周期元素所形成的氢化物稳定性、沸点高低并说明理由____________________________________。
3.[化学——选修有机化学基础]
A~J均为有机化合物,它们之间的转化如下图所示:

实验表明:
①D既能发生银镜反应,又能与金属钠反应放出氢气;
②核磁共振氢谱表明F分子中有三种氢,且其峰面积之比为1∶1∶1;
③G能使溴的四氯化碳溶液褪色;
④1 mol J与足量金属钠反应可放出22.4 L氢气(标准状况)。
请根据以上信息回答下列问题:
(1)A的结构简式为_________(不考虑立体异构),由A生成B的反应类型是_________反应;
(2)D的结构简式为___________________________;
(3)由E生成F的化学方程式为____________,E中的官能团有____________(填名称),与E具有相同官能团的E的同分异构体还有____________(写出结构简式,不考虑立体异构);
(4)G的结构简式为____________________________________;
(5)由I生成J的化学方程式为________________________。
 某校高一化学研究性学习小组对日常生活中的氯气用途进行了调查,了解到氯气可广泛地应用于衣物的漂白、水体的杀菌和消毒等.
某校高一化学研究性学习小组对日常生活中的氯气用途进行了调查,了解到氯气可广泛地应用于衣物的漂白、水体的杀菌和消毒等.(9分)
某中学高一化学兴趣小组的同学,在实验室探究用过量的锌与浓硫酸反应制取SO2。
(1)这样制取的SO2中可能含有的杂质有 和 。
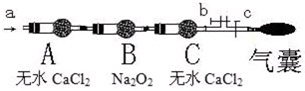
(2)某同学用下列装置连接成一整套实验装置以验证①的判断是否正确,若按气体从左到右流向时,气体流经的各装置导管的编号依次是 → → → → → (用a、b……填写;每套装置只允许使用一次)。
(3)根据②确定的实验过程,请将实验时有关装置中所盛药品、实验现象、结论填入下表:
| 装置 | 所盛药品 | 实验现象 | 结论 |
| B |
|
|
|
| C | CuO固体 |
|
|
| D | 无水CuSO4 |
|
08天津大港一中高三化学第二次月考试卷,化学,15)下列有关化学实验操作中“先”与“后”的说法不正确的是 ( )
A.用排水法收集气体后,先移出导管后撤酒精灯
B.给试管加热时,先均匀加热,后局部加热
C.碱液流到桌子上,先用稀醋酸溶液中和,后用水洗
D.浓硫酸不慎洒到皮肤上,先迅速用水冲洗,后涂上3%~5%的NaHCO3溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com