
̀âÄ¿Áбí(°üÀ¨´đ°¸ºÍ½âÎö)
³ưÈ¥SO2Æø̀åÖĐÉÙÁ¿SO3Æø̀壬ӦѡÓĂ
[¡¡¡¡]
A£®±¥ºÍNaHSO3ÈÜ̉º
B£®±¥ºÍNaOHÈÜ̉º
C£®±¥ºÍH2SO3ÈÜ̉º
D£®Å¨H2SO4
³ưÈ¥SO2Æø̀åÖĐÉÙÁ¿SO3Æø̀壬ӦѡÓĂ£¨¡¡£©
A£®±¥ºÍNaHSO3ÈÜ̉º
B£®±¥ºÍNaOHÈÜ̉º
C£®±¥ºÍH2SO3ÈÜ̉º
D£®Å¨H2SO4

| ¼́ÑéÊÔ¼Á | Ô¤ÆÚÏÖÏóÓë½áÂÛ |
| ×°ÖĂIIIµÄÊÔ¹ÜÖĐ¼ÓÈë×ăÁ¿ 0.5mol£®L-1BaCl2 0.5mol£®L-1BaCl2 £® |
²úÉú´óÁ¿°×É«³Áµí£¬Ö¤Ă÷Æø̀å²úÎïÖĐº¬ÓĐSO3£® |
| ×°ÖĂIVµÄÊÔ¹ÜÖĐ¼ÓÈë×ăÁ¿ 0.01mol£®L-1ËáĐÔKMnO4ÈÜ̉º£¨»̣0.0lmol£®L-1äåË®£© 0.01mol£®L-1ËáĐÔKMnO4ÈÜ̉º£¨»̣0.0lmol£®L-1äåË®£© £® |
ÈôÈÜ̉º×ÏÉ«£¨»̣³ÈÉ«£©ÍÊÈ¥£¬Ö¤Ă÷Æø̀å²úÎïÖĐº¬ÓĐSO2£¬ ÈôÈÜ̉º×ÏÉ«£¨»̣³ÈÉ«£©ÍÊÈ¥£¬Ö¤Ă÷Æø̀å²úÎïÖĐº¬ÓĐSO2£¬ ÈôÈÜ̉º×ÏÉ«£¨»̣³ÈÉ«£©Î̃Ă÷ÏԱ仯£¬Ö¤Ă÷Æø̀å²úÎïÖĐ²»º¬SO2 ÈôÈÜ̉º×ÏÉ«£¨»̣³ÈÉ«£©Î̃Ă÷ÏԱ仯£¬Ö¤Ă÷Æø̀å²úÎïÖĐ²»º¬SO2 £® |
2012Ä궬¼¾£¬Î̉¹ú³ÇÊĐ¿ƠÆøÎÛȾ״¿öÊܵ½ÈËĂǵÄÇ¿Á̉¹Ø×¢£¬ÆäÖĐNOx¡¢CO¡¢SO2ÊÇÖ÷̉ªÎÛȾĐÔÆø̀å¡£
I£®Æû³µÄÚȼ»ú¹¤×÷ʱ·¢ÉúµÄ·´Ó¦ Êǵ¼ÖÂÆû³µÎ² ÆøÖĐº¬ÓĐNOµÄÖØ̉ªỘ̉Ö®̉»¡£
Êǵ¼ÖÂÆû³µÎ² ÆøÖĐº¬ÓĐNOµÄÖØ̉ªỘ̉Ö®̉»¡£
£¨1£©ÓĐÈËÓûÑ¡ÓĂºÏÊʵĴ߻¯¼Á£¬Ê¹·´Ó¦2NO£¨g£©=N2£¨g£©+O2£¨g£©ÄܽϿ́½øĐĐ̉Ô´ïµ½³ưÈ¥NOµÄÄ¿µÄ¡£ÄăÈÏΪ¸Ă·´Ó¦ÄÜ·ñ×Ô·¢½øĐĐ £῭î¡°ÄÜ¡±»̣¡°²»ÄÜ¡±£©¡£
£¨2£©ÀûÓĂ´ß»¯¼¼Êơ¿É½«Æû³µÎ²ÆøÖеÄNOÆø̀åת»¯³ÉÎ̃¶¾Æø̀壬Ïà¹Ø·´Ó¦µÄƽºâ³£Êư¿É±íʾΪ
 £¬´Ë·´Ó¦Îª·ÅÈÈ·´Ó¦¡£ÔÚ̉»¶¨Î¶ÈÏ£¬10LijĂܱƠÈƯÆ÷ÖĐ·¢ÉúÉÏÊö·´Ó¦£¬¸÷ÎïÖʵÄÎïÖʵÄÁ¿µÄ±ä»¯Çé¿öÈçϱí
£¬´Ë·´Ó¦Îª·ÅÈÈ·´Ó¦¡£ÔÚ̉»¶¨Î¶ÈÏ£¬10LijĂܱƠÈƯÆ÷ÖĐ·¢ÉúÉÏÊö·´Ó¦£¬¸÷ÎïÖʵÄÎïÖʵÄÁ¿µÄ±ä»¯Çé¿öÈçϱí

¢Ù¸ù¾ƯÍÁ±íÊư¾Ư¼ÆËă0~4s¼äÓĂNO±íʾµÄƽ¾ùËÙÂÊv£¨NO£©= £»´ïµ½»¯Ñ§Æ½ºâʱÁ½ÖÖ·´Ó¦ÎïµÄת»¯ÂÊÊÇ·ñÏàµÈ £῭î¡°ÏàµÈ¡±»̣¡°²»ÏàµÈ¡±£©¡£
¢ÚÔÚ5~6sʱ£¬ÈôKÔö´ó£¬5sºóƠư·´Ó¦ËÙÂÊ £῭î¡°Ôö´ó¡±»̣¡°¼ơĐ¡¡±£©
¢ÛÔÚ5~6sʱ£¬ÈôK²»±ä£¬̉ÔÉϸ÷ÎïÖʵÄÎïÖʵÄÁ¿±ä»¯Ộ̉¿ÉÄÜÊÇ ¡£
A£®Ñ¡ÓøüÓĐЧµÄ´ß»¯¼Á B£®ËơĐ¡ÈƯÆ÷µÄ̀å»ư
C£®½µµÍCO2Ũ¶È D£®Éư¸ßζÈ
IIΪ̀½¾¿Ạ́ÔÚÑơÆøÖĐȼÉƠµÄ²úÎïÀïÊÇ·ñÓĐSO3£¬Ä³»¯Ñ§ĐËÈ¤Đ¡×éÔÚ¾øÈÈ»·¾³Ï½øĐĐÁ˶¨Á¿ÊµÑé̀½¾¿¡£̀½¾¿ÊµÑéµÄÏà¹ØÊư¾ƯÈçÏÂ
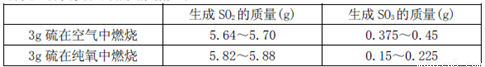
£¨3£©¶ÔÊư¾Ư½øĐĐ·ÖÎö¿ÉÖª£¬µÈÖÊÁ¿µÄẠ́ÔÚ´¿ÑơÖĐȼÉƠ²úÉúµÄSO3±ÈÔÚ¿ƠÆøÖĐȼÉƠ²úÉúµÄSO3 £῭î¡°¶à¡±»̣¡°ÉÙ¡±£©£¬Ộ̉¿ÉÄÜÊÇ ¡£
A£®´¿ÑơÖĐÑơÆøŨ¶È¸ß£¬ÓĐÀûÓÚ»¯Ñ§Æ½ºâ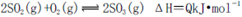 Ị̈Ó̉̉ƶ¯
Ị̈Ó̉̉ƶ¯
B£®»¯Ñ§·´Ó¦
C£®´¿ÑơÖĐÑơÆøŨ¶È¸ß£¬µ¥Î»Ê±¼äÄÚ·¢ÈÈÁ¿´ó£¬ÖÂʹ·´Ó¦̀åϵµÄζȽϸߣ¬²»ÀûÓÚ»¯Ñ§Æ½ºâ
 Ị̈Ó̉̉ƶ¯
Ị̈Ó̉̉ƶ¯
D£®3gẠ́ÔÚ´¿ÑơÖĐȼÉƠ±È3gẠ́ÔÚ¿ƠÆøÖĐȼÉƠ·Å³öµÄÈÈÁ¿¶à£¬²»ÀûÓÚ»¯Ñ§Æ½ºâ
 Ị̈Ó̉̉ƶ¯
Ị̈Ó̉̉ƶ¯
¹ú¼ÊÑ§Đ£ÓÅÑ¡ - Á·Ï°²áÁбí - ÊỒâÁбí
º₫±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨Æ½̀¨ | ÍøÉÏÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | µçĐÅƠ©Æ¾Ù±¨×¨Çø | ÉæÀúÊ·ĐéÎ̃Ö÷̉åÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com