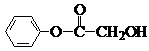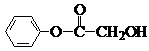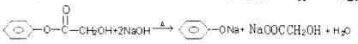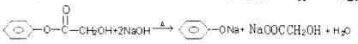化合物A、B均是分子式为C
8H
8O
3的无色液体,均难溶于水.从A、B开始,可发生图示的一系列反应(反应中的无机物已部分略去),E的苯环上的一元硝基化物只有两种,K可发生银镜反应.

(1)写出A和K的结构简式:A
K
HCOOCH3
HCOOCH3
;X与K互为同分异构体且也可发生银镜反应,则X所含官能团的为
.
(2)上图a-i的反应中,属于酯化反应的有
e、i
e、i
(填字母)
(3)写出反应a的化学方程式是
.
(4)已知CH
3COONa+NaOH
CH
4↑+Na
2CO
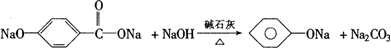
3,请完成E→D的反应方程式
.
(5)实验室配制银氨溶液的主要操作是
在洁净的试管里加入1mL2%的硝酸银溶液,然后一边摇动试管一边逐滴滴入2%的稀氨水,至最初产生的沉淀恰好完全溶解为止,即配得银氨溶液
在洁净的试管里加入1mL2%的硝酸银溶液,然后一边摇动试管一边逐滴滴入2%的稀氨水,至最初产生的沉淀恰好完全溶解为止,即配得银氨溶液
写出K与银氨溶液反应的离子方程式为
HCOOCH
3+2Ag(NH
3)
2++2OH
-CH
3OH+CO
32-+2NH
4++2Ag↓+2NH
3HCOOCH
3+2Ag(NH
3)
2++2OH
-CH
3OH+CO
32-+2NH
4++2Ag↓+2NH
3(6)芒香族化合物W与A互为同分异构体且满足以下条件:①1molW能与含3molNaOH
的溶液恰好反应,②苯环上不直接连甲基,则符合上述条件的W的同分异构体有
10
10
种.