
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)


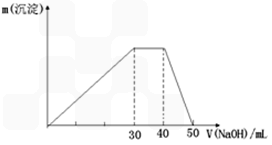
Θ®9Ζ÷Θ©Ά≠ΦΑΤδΚœΫπ «»ΥάύΉν‘γ Ι”ΟΒΡΫπ τ≤ΡΝœΓΘ
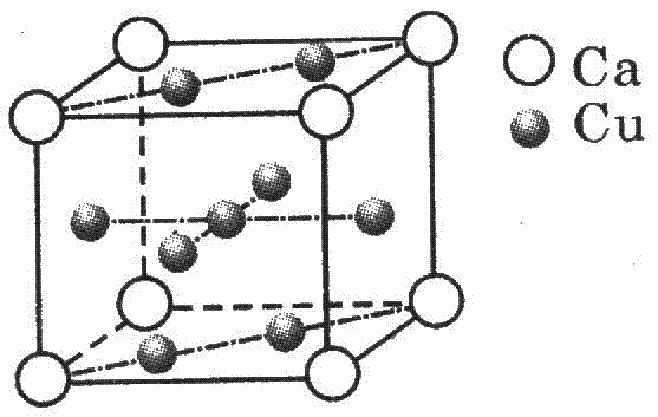 (1)Ά≠‘≠Ή”ΒΡΚΥΆβΒγΉ”≈≈≤Φ Ϋ « ΓΘ
(1)Ά≠‘≠Ή”ΒΡΚΥΆβΒγΉ”≈≈≤Φ Ϋ « ΓΘ
(2)»γΆΦ «Ϋπ τCaΚΆCuΥυ–Έ≥…ΒΡΡ≥÷÷ΚœΫπΒΡΨßΑϊΫαΙΙ Ψ“βΆΦΘ§‘ρΗΟΚœΫπ÷–CaΚΆCuΒΡ‘≠Ή”Ηω ΐ±»ΈΣ ΓΘ
(3)Cu2+Ρή”κNH3ΓΔH2OΓΔC1Θ≠Β»–Έ≥…≈δΈΜ ΐΈΣ4ΒΡ≈δΚœΈοΓΘ
ΔΌ[Cu(NH3)4]2+ΨΏ”–Ε‘≥ΤΒΡΩ’ΦδΙΙ–ΆΘ§[Cu(NH3)4]2+÷–ΒΡΝΫΗωNH3±ΜΝΫΗωClΘ≠»Γ¥ζΘ§ΡήΒΟΒΫΝΫ÷÷≤ΜΆ§ΫαΙΙΒΡ≤ζΈοΘ§‘ρ[Cu(NH3)4]2+ΒΡΩ’ΦδΙΙ–ΆΈΣ ΓΘ
ΔΎΡ≥÷÷Κ§Cu2+ΒΡΜ·ΚœΈοΩ…¥ΏΜ·±ϊœ©¥Φ÷Τ±Η±ϊ»©ΒΡΖ¥”ΠΘΚHOCH2CH=CH2ΓζCH3CH2CHOΓΘ‘Ύ±ϊœ©¥ΦΖ÷Ή”÷–ΖΔ…ζΡ≥÷÷ΖΫ Ϋ‘”Μ·ΒΡΧΦ‘≠Ή” ΐΘ§ «±ϊ»©Ζ÷Ή”÷–ΖΔ…ζΆ§―υΖΫ Ϋ‘”Μ·ΒΡΧΦ‘≠Ή” ΐΒΡ2±ΕΘ§‘ρ’βάύΧΦ‘≠Ή”ΒΡ‘”Μ·ΖΫ ΫΈΣ ΓΘ
(4)CaOΨßΧεΒΡΫαΙΙ”κNaClœύΆ§Θ§CaOΨßΧε÷–Ca2+ΒΡ≈δΈΜ ΐΈΣ ΓΘ
ΨßΗώΡήΖ÷±πΈΣΘΚCaOΈΣΘ≠3401 kJ?molΘ≠1ΓΔNaClΈΣΘ≠786 kJ?molΘ≠1ΓΘΒΦ÷¬ΝΫ’ΏΨßΗώΡή≤ν“λΒΡ÷ς“Σ‘≠“ρ « ΓΘ
(5)ΦΌΕ®Χζ”–ΦρΒΞΝΔΖΫΓΔΧε–ΡΝΔΖΫ(bcp)ΓΔΟφ–ΡΝΔΖΫ(ccp)»ΐ÷÷Ά§ΥΊ“λ–ΈΧεΘ§»ΐ÷÷ΨßΧε‘Ύ≤ΜΆ§Έ¬Ε»œ¬ΡήΖΔ…ζœύΜΞΉΣΜ·ΓΘ»τ»ΐ÷÷Ά§ΥΊ“λ–ΈΧεΨßΑϊ±Ώ≥ΛΖ÷±πΈΣa cmΘ§ b cmΘ§c cm‘ρ»ΐ÷÷ΨßΧεΟήΕ»±»ΈΣ ΓΘ
ν―ΚΆν―ΒΡΚœΫπ“―±ΜΙψΖΚ”Ο”Ύ÷Τ‘λΒγ―ΕΤς≤ΡΓΔ»Υ‘λΙ«ςάΓΔΜ·ΙΛ…η±ΗΓΔΖ…ΜζΒ»ΚΫΧλΚΫΩ’≤ΡΝœΘ§±Μ”ΰΈΣΓΑΈ¥ά¥ άΫγΒΡΫπ τΓ±ΓΘ ‘ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
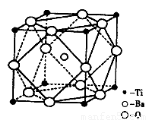
Θ®1Θ©ν―”– ΝΫ÷÷‘≠Ή”Θ§ΥϋΟ«ΜΞ≥ΤΈΣ____ΓΘ‘ΣΥΊ‘Ύ‘ΣΥΊ÷ήΤΎ±μ÷–ΒΡΈΜ÷Ο «ΒΎ_____÷ήΤΎΘ§ΒΎ____ΉεΘΜΜυΧ§‘≠Ή”ΒΡΒγΉ”≈≈≤Φ ΫΈΣ_____ΘΜΑ¥ΒγΉ”≈≈≤ΦTi‘ΣΥΊ‘Ύ‘ΣΥΊ÷ήΤΎ±μΖ÷«χ÷– τ”Ύ_____«χ‘ΣΥΊΓΘ
ΝΫ÷÷‘≠Ή”Θ§ΥϋΟ«ΜΞ≥ΤΈΣ____ΓΘ‘ΣΥΊ‘Ύ‘ΣΥΊ÷ήΤΎ±μ÷–ΒΡΈΜ÷Ο «ΒΎ_____÷ήΤΎΘ§ΒΎ____ΉεΘΜΜυΧ§‘≠Ή”ΒΡΒγΉ”≈≈≤Φ ΫΈΣ_____ΘΜΑ¥ΒγΉ”≈≈≤ΦTi‘ΣΥΊ‘Ύ‘ΣΥΊ÷ήΤΎ±μΖ÷«χ÷– τ”Ύ_____«χ‘ΣΥΊΓΘ
Θ®2Θ©ΤΪν―Υα±Β‘Ύ–Γ–Ά±δ―ΙΤςΓΔΜΑΆ≤ΚΆά©“τΤς÷–ΕΦ”–”Π”ΟΓΘΤΪν―Υα±ΒΨßΧε÷–ΨßΑϊΒΡΫαΙΙ»γΆΦΥυ ΨΘ§ΥϋΒΡΜ·―ß Ϋ «______Θ§
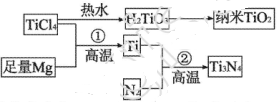
Θ®3Θ©ΒΣΜ·ν―(Ti3N4)ΈΣΫπΜΤ…ΪΨßΧεΘ§”…”ΎΨΏ”–Νν»Υ¬ζ“βΒΡΖ¬Ϋπ–ßΙϊΘ§‘Ϋά¥‘ΫΕύΒΊ≥…ΈΣΜΤΫπΉΑ ΈΒΡΧφ¥ζΤΖΓΘ“‘TiCl4ΈΣ‘≠ΝœΘ§Ψ≠Ιΐ“ΜœΒΝ–Ζ¥”ΠΘ§Ω…“‘÷ΤTi3N4ΚΆΡ…ΟΉTiO2
 ΓΘ
ΓΘ
ΔΌTi3N4÷–‘ΣΥΊΒΡΜ·ΚœΦέΈΣ_____ΓΘTiCl4Ζ÷Ή”÷–4Ηω¬»‘≠Ή”≤Μ‘ΎΆ§“ΜΤΫΟφ…œΘ§‘ρTiCl4ΒΡΩ’ΦδΙΙ–ΆΈΣ______ΓΘ
ΔΎΖ¥”ΠΔΌΈΣ÷ΟΜΜΖ¥”ΠΓΔΗΟΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣ______ΓΘ
ΔέΡ…ΟΉTiO2 «“Μ÷÷”Π”ΟΙψΖΚΒΡ¥ΏΜ·ΦΝΘ§Ρ…ΟΉTiO2¥ΏΜ·ΒΡ“ΜΗω Βάΐ»γœ¬ΘΚ

Μ·ΚœΈοΦΉΒΡΖ÷Ή”÷–≤…»Γ ‘”Μ·ΒΡΧΦ‘≠Ή”Ηω ΐΈΣ_____Θ§Μ·ΚœΈο““÷–≤…»Γ
‘”Μ·ΒΡΧΦ‘≠Ή”Ηω ΐΈΣ_____Θ§Μ·ΚœΈο““÷–≤…»Γ ‘”Μ·ΒΡ‘≠Ή”ΒΡΒΎ“ΜΒγάκΡή”…¥σΒΫ–ΓΒΡΥ≥–ρΈΣ_____ΓΘ
‘”Μ·ΒΡ‘≠Ή”ΒΡΒΎ“ΜΒγάκΡή”…¥σΒΫ–ΓΒΡΥ≥–ρΈΣ_____ΓΘ
Δή”–“Μ÷÷ΒΣΜ·ν―ΨßΧεΒΡΨßΑϊ»γΆΦΥυ ΨΘ§ΗΟΒΣΜ·ν―ΨßΑϊ÷–Κ§”–______ΗωN‘≠Ή”Θ§ΨßΑϊ÷–NΓΔTi÷°ΦδΒΡΉνΫϋΨύάκΈΣa pmΘ§‘ρΗΟΒΣΜ·ν―ΒΡΟήΕ»ΈΣ______gΘ° (NAΈΣΑΔΖϋΦ”Β¬¬ό≥Θ ΐΒΡ ΐ÷ΒΘ§÷ΜΝ–Υψ Ϋ)ΓΘ
(NAΈΣΑΔΖϋΦ”Β¬¬ό≥Θ ΐΒΡ ΐ÷ΒΘ§÷ΜΝ–Υψ Ϋ)ΓΘ

 ΝΫ÷÷‘≠Ή”Θ§ΥϋΟ«ΜΞ≥ΤΈΣ____ΓΘ‘ΣΥΊ‘Ύ‘ΣΥΊ÷ήΤΎ±μ÷–ΒΡΈΜ÷Ο «ΒΎ_____÷ήΤΎΘ§ΒΎ____ΉεΘΜΜυΧ§‘≠Ή”ΒΡΒγΉ”≈≈≤Φ ΫΈΣ_____ΘΜΑ¥ΒγΉ”≈≈≤ΦTi‘ΣΥΊ‘Ύ‘ΣΥΊ÷ήΤΎ±μΖ÷«χ÷– τ”Ύ_____«χ‘ΣΥΊΓΘ
ΝΫ÷÷‘≠Ή”Θ§ΥϋΟ«ΜΞ≥ΤΈΣ____ΓΘ‘ΣΥΊ‘Ύ‘ΣΥΊ÷ήΤΎ±μ÷–ΒΡΈΜ÷Ο «ΒΎ_____÷ήΤΎΘ§ΒΎ____ΉεΘΜΜυΧ§‘≠Ή”ΒΡΒγΉ”≈≈≤Φ ΫΈΣ_____ΘΜΑ¥ΒγΉ”≈≈≤ΦTi‘ΣΥΊ‘Ύ‘ΣΥΊ÷ήΤΎ±μΖ÷«χ÷– τ”Ύ_____«χ‘ΣΥΊΓΘ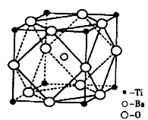
 ΓΘ
ΓΘ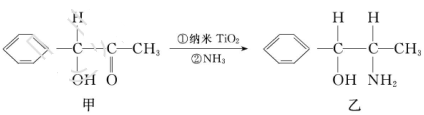
 ‘”Μ·ΒΡΧΦ‘≠Ή”Ηω ΐΈΣ_____Θ§Μ·ΚœΈο““÷–≤…»Γ
‘”Μ·ΒΡΧΦ‘≠Ή”Ηω ΐΈΣ_____Θ§Μ·ΚœΈο““÷–≤…»Γ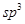 ‘”Μ·ΒΡ‘≠Ή”ΒΡΒΎ“ΜΒγάκΡή”…¥σΒΫ–ΓΒΡΥ≥–ρΈΣ_____ΓΘ
‘”Μ·ΒΡ‘≠Ή”ΒΡΒΎ“ΜΒγάκΡή”…¥σΒΫ–ΓΒΡΥ≥–ρΈΣ_____ΓΘ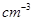 (NAΈΣΑΔΖϋΦ”Β¬¬ό≥Θ ΐΒΡ ΐ÷ΒΘ§÷ΜΝ–Υψ Ϋ)ΓΘ
(NAΈΣΑΔΖϋΦ”Β¬¬ό≥Θ ΐΒΡ ΐ÷ΒΘ§÷ΜΝ–Υψ Ϋ)ΓΘ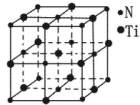
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com