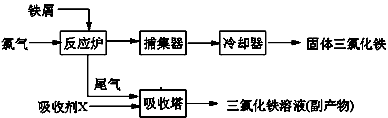
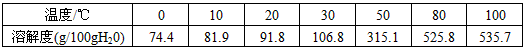氯化铁是常见的水处理剂,无水FeCl
3的熔点为555K、沸点为588K.工业上制备无水FeCl
3的一种工艺如下:
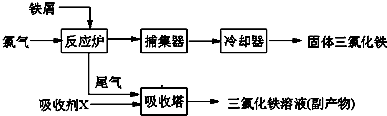
(1)试写出吸收塔中反应的离子方程式:
2Fe2++Cl2=2Fe3++2Cl-
2Fe2++Cl2=2Fe3++2Cl-
.
(2)已知六水合氯化铁在水中的溶解度如下:
| 温度/℃ |
0 |
10 |
20 |
30 |
50 |
80 |
100 |
| 溶解度(g/100gH20) |
74.4 |
81.9 |
91.8 |
106.8 |
315.1 |
525.8 |
535.7 |
从FeCl
3溶液中获得FeCl
3?6H
2O的方法是:
加入少量盐酸加热浓缩,再冷却结晶
加入少量盐酸加热浓缩,再冷却结晶
.
(3)捕集器中温度超过673K,存在相对分子质量为325的物质,该物质的分子式为:
Fe2Cl6
Fe2Cl6
.
(4)室温时在FeCl
3溶液中滴加NaOH溶液,当溶液pH为2.7时,Fe
3+开始沉淀;当溶液pH为4时,c(Fe
3+)=
1.1×10-6
1.1×10-6
mol/L(已知:Ksp[Fe(OH)
3]=1.1×10
-36).
(5)FeCl
3的质量分数通常可用碘量法测定:称取m克无水氯化铁样品,溶于稀盐酸,再转移到100mL容量瓶,用蒸馏水定容;取出10mL,加入稍过量的KI溶液,充分反应后,滴入某一指示剂并用c mol/L Na
2S
2O
3溶液滴定用去V mL.(已知:I
2+2S
2O
32-=2I
-+S
4O
62-)
①滴定终点的现象是:
滴入最后一滴,溶液颜色由蓝色变为无色,半分钟内不再变色
滴入最后一滴,溶液颜色由蓝色变为无色,半分钟内不再变色
.
②样品中氯化铁的质量分数为:
.
③某同学根据上述方案,使用上述(2)中获得的FeCl
3?6H
2O样品代替无水氯化铁样品进行测定.通过计算发现产品中的质量分数大于100%,其原因可能是
FeCl3?6H2O烘干时失去了部分结晶水
FeCl3?6H2O烘干时失去了部分结晶水
.

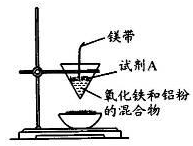
 CO(g)+H2(g)达到平衡时,测得气体的总质量为m g,混合气体的物质的量为n mol。当改变条件使平衡向左移动达到新的平衡时,混合气体物质的量的变化值△n=x mol,且m>12x,n>x,请回答下列问题:
CO(g)+H2(g)达到平衡时,测得气体的总质量为m g,混合气体的物质的量为n mol。当改变条件使平衡向左移动达到新的平衡时,混合气体物质的量的变化值△n=x mol,且m>12x,n>x,请回答下列问题: