
题目列表(包括答案和解析)
(2)58.5 g NaCl配成1 L溶液,其物质的量浓度为__________ mol·L-1。
(3)标准状况下,22.4 L HCl配成0.5 L盐酸,其物质的量浓度为__________ mol·L-1。
(4)2 mol NaOH配成200 mL溶液,其物质的量浓度为__________mol·L-1。
(5)物质的量浓度为2 mol·L-1 的硫酸溶液500 mL,含硫酸的物质的量为__________mol。
(6)10mol HCl能配成__________L物质的量浓度为2 mol·L-1的盐酸。
(1)用甲烷制氢是一种廉价的制氢方法。有关的热化学方程式如下:
CH4(g)+1/2O2(g)
 CO(g)+2H2(g);△H= -36kJ/mol……… ①
CO(g)+2H2(g);△H= -36kJ/mol……… ①
CH4(g)+H2O(g)
 CO(g)+3H2(g);△H= +216kJ/mol…………②
CO(g)+3H2(g);△H= +216kJ/mol…………②
①下列说法正确的是 ____
A.2H2O(l)=2H2(g)+O2(g) △H=+504kJ/mol
B.当反应①中υ(CH4)正=υ(CO)正时,表明该反应达平衡状态
C.其它条件不变时,增大体系压强,反应①②中甲烷的转化率均增大
D.为维持恒定温度(不考虑热量损失),某反应器中同时发生反应①与②时,消耗甲
烷的物质的量之比为6∶1
②某温度下,在100L反应器中充入甲烷和水蒸汽的物质的量分别为100mol和300mol时,假定只发生反应CH4(g)+H2O(g)  CO(g)+3H2(g)。当甲烷的转化率为0.5时,此时平衡常数为 _______
CO(g)+3H2(g)。当甲烷的转化率为0.5时,此时平衡常数为 _______
(2)发蓝液是由NaNO3、NaNO2及NaOH配成的,在加热条件下,通过三步反应使铁表面生成一层致密的Fe3O4:
3Fe+NaNO2+5NaOH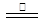 3Na2FeO2+H2O+NH3↑…………①;
3Na2FeO2+H2O+NH3↑…………①;
8Fe+3NaNO3+5NaOH+2H2O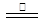 4Na2Fe2O4+3NH3↑……②;
4Na2Fe2O4+3NH3↑……②;
以及第三步生成四氧化三铁。请补充第三步反应的方程式并配平: __________________
 CO(g)+2H2(g);△H= -36kJ/mol ①
CO(g)+2H2(g);△H= -36kJ/mol ①  CO(g)+3H2(g);△H= +216kJ/mol ②
CO(g)+3H2(g);△H= +216kJ/mol ②  CO(g)+3H2(g)。当甲烷的转化率为0.5时,此时平衡常数为__________。
CO(g)+3H2(g)。当甲烷的转化率为0.5时,此时平衡常数为__________。 Na2FeO2+H2O+NH3↑ ①;
Na2FeO2+H2O+NH3↑ ①; 4Na2Fe2O4+3NH3↑ ②;
4Na2Fe2O4+3NH3↑ ②;
 CO(g)+2H2(g);△H=-36kJ/mol……… ①
CO(g)+2H2(g);△H=-36kJ/mol……… ①  CO(g)+3H2(g);△H=+216kJ/mol………②
CO(g)+3H2(g);△H=+216kJ/mol………②  CO(g)+3H2(g)。当甲烷的转化率为0.5时,此时平衡常数为______________。
CO(g)+3H2(g)。当甲烷的转化率为0.5时,此时平衡常数为______________。 3Na2FeO2+H2O+NH3↑…………①;
3Na2FeO2+H2O+NH3↑…………①;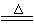 4Na2Fe2O4+3NH3↑……②;
4Na2Fe2O4+3NH3↑……②;
用经过准确称量的NaOH固体配制250 mL 0.2 mol/L的NaOH溶液,在下列实验仪器中不必使用的是(填写代号)________;还缺少的实验仪器是(填写仪器名称)________.
①托盘天平
②50 mL量筒
③500 mL容量瓶
④250 mL烧杯
⑤玻璃棒
⑥500 mL试剂瓶
实验室里需要480 mL 0.1 mol·L-1的硫酸铜溶液,现取500 mL的容量瓶进行配制,以下操作中正确的是________.
A.称取8.0 g硫酸铜,加入500 mL水
B.称取12.0 g胆矾配成500 mL溶液
C.称取12.5 g胆矾配成500 mL溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com