
题目列表(包括答案和解析)
|
t℃时CuSO4的溶解度是Sg,其饱和溶液密度为d g/cm3,物质的量浓度为c mol/L.向足量饱和溶液中加入mg无水CuSO4或蒸发掉n g水后恢复到t℃,均能获得W g胆矾晶体,下列关系式正确的是 | |
| [ ] | |
A. |
|
B. |
|
C. |
|
D. |
|
体积为V mL、密度为ρ g/cm3的溶液,含有相对分子质量为M的溶质m g,其物质的量浓度为c mol/L,溶质的质量分数为W%,下列表示式中正确的是( )
A.c=![]() B.m=
B.m=![]() C.W%=
C.W%=![]() % D.c=
% D.c=![]()
在密闭容器中加入4mol A和2mol
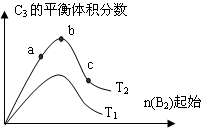
B发生如下反应2A(气)+B(气)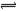 3C(气)+D(气)达到平衡时,C的浓度为p
mol/L,若温度和体积不变时按下列配比作为起始物质,达到平衡后C浓度仍为p mol/L的是:
3C(气)+D(气)达到平衡时,C的浓度为p
mol/L,若温度和体积不变时按下列配比作为起始物质,达到平衡后C浓度仍为p mol/L的是:
A. 2molA+1molB B. 2molA+1molB+3molC +1moD
C. 3molC+1molD D. 6molC+2molD
(12分)已知2A2(g)+B2(g) 2C3(g);△H=-Q1 kJ/mol(Q1>0),在一个有催化剂的固定
容积的容器中加入2 molA2和1 molB2,在500℃时充分反应,达平衡后C3的浓度为
w mol/L,放出热量Q2 kJ。
(1)若在原来的容器中,只加入2mol C3,500℃时充分反应达平衡后,吸收热量Q3 kJ,C3浓度 (填>、=、<)w mol/L,Q1、Q2、Q3 之间满足何种关系 (用代数式表示)。
(2)能说明该反应已经达到平衡状态的是 。
 a.v(C3)=2 v (B2); b.容器内压强保持不变
a.v(C3)=2 v (B2); b.容器内压强保持不变
c.v逆(A2)=2 v正(B2) d.容器内的密度保持不变
(3)改变某一条件,得到如图的变化规律(图中T表示温度,n表示物质的量),可得出的结论正确的是 ;
A.反应速率c>b>a
B.达到平衡时A2的转化率大小为:b>a>c
C.T2>T1
D.b点时,平衡体系中A、B原子数之比接近2∶1
(4)若将上述容器改为恒压容器(反应前体积相同),起始时加入2molA2和l molB2,500℃时充分反应达平衡后,放出热量Q4 kJ,则Q2 Q4 ( 填 > 、 = 、 < ),理由是 。
在体积和温度不变的密闭容器中充入1mol H2O蒸气和足量铁粉,建立平衡
3Fe(s)+4H2O(g)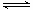 Fe3O4(s)+4H2(g)之后,测得H2O蒸气的分解率为x%,浓度为c1mol/L。若再充人1mol H2O蒸气,建立新的平衡后.又测得H2O蒸气的分解率为y%,浓度为C2 mol/L。则下列关系正确的是
Fe3O4(s)+4H2(g)之后,测得H2O蒸气的分解率为x%,浓度为c1mol/L。若再充人1mol H2O蒸气,建立新的平衡后.又测得H2O蒸气的分解率为y%,浓度为C2 mol/L。则下列关系正确的是
A.x>y,c1>c2 B.x<y,c1<c2 C.x=y,c1 =c2 D.x=y,c1<c2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com