
题目列表(包括答案和解析)



| ||
| ||
| 5 |
| 2 |
| 5 |
| 2 |

| ||
| ||
近年来特大地震灾害频繁发生,地震过后,饮用水的
消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一.漂白粉是常用的消毒剂.工业上制漂白粉有以下工序:(1)海水晒盐.
(2)粗盐提纯:粗盐中主要含有MgCl2、Na2SO4和FeCl3杂质,设计如下方案:
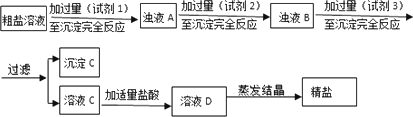
①试剂1
~试剂3依次为:________、________、________.②沉淀C含有BaSO4、Mg(OH)2还有________(用化学式表示).
(3)电解法制氯气:观察下图,回答:
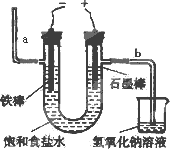
①通电后,________(填a或b)侧产生氢气.
②此电解反应的化学方程式为________.
(4)制取漂白粉:将氯气通入消石灰(Ca(OH)2)中反应,
化学方程式为:________.(5)实验室加热MnO2和浓盐酸混合物来制取氯气.
①反应原理:MnO2+HCl(浓)![]() MnCl2+Cl2↑+H2O(未配平)
MnCl2+Cl2↑+H2O(未配平)
若有8
.7克的MnO2被还原,则有________mol HCl被氧化.②在下列各装置中,选用必要的装置,制备纯净干燥的Cl2,并按从左到右的顺序连接仪器,用接口字母按顺序连接为:
________.(顺序错误不得分)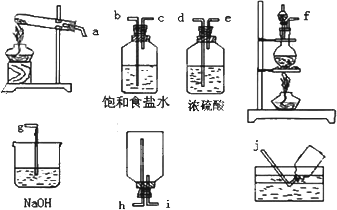
(11分)近年来特大地震灾害频繁发生,地震过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。工业上制漂白粉有以下工序:
(1)海水晒盐。
(2)粗盐提纯:粗盐中主要含有MgCl2、Na2SO4和FeCl3杂质,设计如下方案:
①试剂1~试剂3依次为: . . 。
②沉淀C含有BaSO4、Mg(OH)2还有 (用化学式表示)。
(3)电解法制氯气:观察下图,回答:
①通电后, (填a或b)侧产生氢气。
②此电解反应的化学方程式为 。
(4)制取漂白粉:将氯气通入消石灰(Ca(OH)2)中反应,化学方程式为: 。
(5)实验室加热MnO2和浓盐酸混合物来制取氯气。
① 若有8.7克的MnO2被还原,则有 molHCl被氧化。
②在下列各装置中,选用必要的装置,制备纯净干燥的Cl2,并按从左到右的顺序连接仪器,用接口字母按顺序连接为: 。(顺序错误不得分)
(11分)近年来特大地震灾害频繁发生,地震过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。工业上制漂白粉有以下工序:
(1)海水晒盐。
(2)粗盐提纯:粗盐中主要含有MgCl2、Na2SO4和FeCl3杂质,设计如下方案:
①试剂1~试剂3依次为: . . 。
②沉淀C含有BaSO4、Mg(OH)2还有 (用化学式表示)。
(3)电解法制氯气:观察下图,回答:
①通电后, (填a或b)侧产生氢气。
②此电解反应的化学方程式为 。
(4)制取漂白粉:将氯气通入消石灰(Ca(OH)2)中反应,化学方程式为: 。
(5)实验室加热MnO2和浓盐酸混合物来制取氯气。
① 若有8.7克的MnO2被还原,则有 molHCl被氧化。
②在下列各装置中,选用必要的装置,制备纯净干燥的Cl2,并按从左到右的顺序连接仪器,用接口字母按顺序连接为: 。(顺序错误不得分)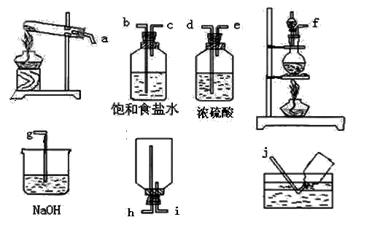
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com