
题目列表(包括答案和解析)
 [化学--选修物质结构]
[化学--选修物质结构]选做题
从以下两道题中任选一道做。
1.光催化制氢是化学研究的热点之一。科学家利用含有吡啶环(吡啶的结构式为![]() ,其性质类似于苯)的化合物Ⅱ作为中间体,实现了循环法制氢,示意图如下(仅列出部分反应条件):
,其性质类似于苯)的化合物Ⅱ作为中间体,实现了循环法制氢,示意图如下(仅列出部分反应条件):

(1)化合物Ⅱ的分子式为________________________________________。
(2)化合物Ⅰ合成方法如下(反应条件略,除化合物Ⅲ的结构未标明外,反应式已配平):
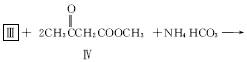
![]()
化合物Ⅲ的名称是_______________________。
(3)用化合物Ⅴ(结构式见下图)代替Ⅲ作原料,也能进行类似的上述反应,所得有机产物的结构式为____________________。

(4)下列说法正确的是________________(填字母)。
A.化合物Ⅴ的名称是间羟基苯甲醛,或2羟基苯甲醛
B.化合物Ⅰ具有还原性;Ⅱ具有氧化性,但能被酸性高锰酸钾溶液氧化
C.化合物Ⅰ、Ⅱ、Ⅳ都可发生水解反应
D.化合物Ⅴ遇三氯化铁显色,还可发生氧化反应,但不能发生还原反应
(5)吡啶甲酸酯可作为金属离子的萃取剂。2吡啶甲酸正丁酯(Ⅵ)的结构式见下图,其合成原料2吡啶甲酸的结构式为__________________;Ⅵ的同分异构体中,吡啶环上只有一个氢原子被取代的吡啶甲酸酯类同分异构体有____________________种。

Ⅵ
2.铜单质及其化合物在很多领域有重要用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂。
(1)Cu位于元素周期表第ⅠB族。Cu2+的核外电子排布式为_____________________。
(2)下图是铜的某种氧化物的晶胞结构示意图,可确定该晶胞中阴离子的个数为________。

(3)胆矾CuSO4·5H2O可写成[Cu(H2O)4]SO4·H2O,其结构示意图如下:

下列说法正确的是_________________(填字母)。
A.在上述结构示意图中,所有氧原子都采用sp3杂化
B.在上述结构示意图中,存在配位键、共价键和离子键
C.胆矾是分子晶体,分子间存在氢键
D.胆矾中的水在不同温度下会分步失去
(4)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是_____________________。
(5)Cu2O的熔点比Cu2S的______________(填“高”或“低”),请解释原因____________________________。
@@1. (1)C11H13NO4 (2)甲醛
(3)
(4)BC
(5)![]() 12
12
A.往氯化铝溶液中加入过量氨水:Al3++3OH-====Al(OH)3↓
B.往硫酸铜溶液中加入过量氢氧化钡:Ba2++SO![]() ====BaSO4↓
====BaSO4↓
C.往澄清石灰水溶液中通入过量二氧化碳:OH-+CO2====HCO![]()
D.往碳酸氢钙溶液中加入过量的氢氧化钠溶液:Ca2++HCO![]() +OH-====CaCO3↓+H2O
+OH-====CaCO3↓+H2O
发展煤的液化技术被纳入 “十二五”规划,中科院山西煤化所有关煤液化技术的高效催化剂研发项目近日已获批复。已知:煤可以先转化为一氧化碳和氢气,再在催化剂作用下合成甲醇,从而实现液化。
(1)根据等电子原理,写出CO分子的结构式 。
 (2)煤炭液化所用的一种催化剂含有铜元素,写出基态铜原子的核外电子排布简式 。
(2)煤炭液化所用的一种催化剂含有铜元素,写出基态铜原子的核外电子排布简式 。
(3)右图是铜的某种氧化物的晶胞结构示意图(顶角和体心是氧),可确定该氧化物的化学式为 。
(4)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知NF3与NH3的结构类似,但NF3不易与Cu2+形成配离子,其主要原因是 。
(5)煤液化获得甲醇,再经催化氧化可得到重要工业原料甲醛,甲醇的沸点比甲醛的高,其主要原因是 ;甲醛分子中碳原子轨道的杂化类型为 ; 1mol甲醛分子中σ键的数目为 。
A.往AgNO3溶液中滴加过量氨水:
Ag++2NH3·H2O====[Ag(NH3)2]++2H2O
B.在硫酸铜溶液中加入氢氧化钡溶液:Ba2++![]() ====BaSO4↓
====BaSO4↓
C.钠与水反应:2Na+2H2O====2Na++2OH-+H2↑
D.在碳酸氢钙溶液中加入过量的NaOH溶液:
Ca2++2![]() +2OH-====CaCO3↓+2H2O+
+2OH-====CaCO3↓+2H2O+![]()
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com