
题目列表(包括答案和解析)
(10分)在常温常压下,可利用下列装置来测定气体体积,抽气装置E用以调节装置中的气压差,减小实验误差。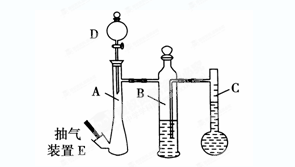
(1)若称取0.113g镁带与10.00 mL稀硫酸(足量)完全反应制取氢气,并测定1mol H2的体积(在常温常压下测定)。反应结束时C中的液面刻度为128.00 mL(A中未加硫酸时C中无液体),则得此条件下1mol H2的体积为________L(精确到0.001)。
(2)上述测出1mol H2的体积比该温度和压强下的理论值偏高的原因是(假设操作和装置都无问题)________(选填编号,下同)
A.未冷却到室温 B.反应太快
C.装置气密性不好 D.B装置漏气
(3)若利用上述装置测定CO2的气体摩尔体积。
①B中所盛放的液体应为________。
A.饱和Na2CO3溶液 B.饱和NaHCO3溶液
C.水 D.澄清石灰水
②仪器A、D中盛放的试剂应为________。
A.大理石,浓盐酸 B.纯碳酸钠,稀硫酸
C.纯碳酸钙,稀硫酸 D.纯碳酸钠,稀盐酸
(4)用以上装置测出的气体摩尔体积均比理论值大,你认为减小实验误差可行的措施是_______。
A.把A装置浸入盛水(常温)的水槽中
B.减小酸的浓度
C.把A装置浸入盛热水的水槽中
D.增大酸的浓度
现分步实验如下:在A溶液中通入适量B气体,溶液酸性显著增强;继续加硝酸钡溶液反应,得到一种不溶于稀硝酸的白色沉淀;过滤,滤液无色;再向滤液中加入硝 酸银溶液,析出另一种不溶于稀硝酸的白色沉淀。回答下列问题。
(1)写出A、B两种气体的名称:A________,B________。
(2)写出上述各步实验中的化学方程式,属离子反应的写离子方程式。
现做如下实验:在A的溶液中通入适量B气体,溶液的酸性显著加强,向溶液中加Ba(NO3)2溶液,得到一种白色沉淀,到不再反应为止,过在滤液中继续加AgNO溶液又产生不溶于稀HNO3的白色沉淀。
(l)写出A、B两种气体的化学式:A:________,B:________。
(2)用化学方程式或离子方程式解释加Ba(NO3)2溶液产生沉淀的原理。
A和B在常温下都是气体,A和B在空气中都不能被点燃,A的式量比B大。
现分步实验如下:在A溶液中通入适量B气体,溶液酸性显著增强;继续加硝酸钡溶液反应,得到一种不溶于稀硝酸的白色沉淀;过滤,滤液无色;再向滤液中加入硝 酸银溶液,析出另一种不溶于稀硝酸的白色沉淀。回答下列问题。
(1)写出A、B两种气体的名称:A________,B________。
(2)写出上述各步实验中的化学方程式,属离子反应的写离子方程式。
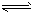 2NO2 △H>0)
2NO2 △H>0)湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com