
题目列表(包括答案和解析)
(1)配制250 mL 0.1 mol·L-1的盐酸溶液
应称量盐酸体积/mL | 应选用容量瓶的规格/mL | 除容量瓶外还需要的其他仪器 |
|
|
|
(2)容量瓶上除有刻度线外还应标有_________,在使用前必须检查容量瓶是否完好以及_________ (填容量瓶的受检部位)处是否漏水。
(3)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)__________。
A.用30 mL水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30 mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入250 mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度2—
(4)操作A中,将洗涤液都移入容量瓶,其目的是____________________。溶液注入容量瓶前需恢复到室温,这是因为____________________。
(5)若出现如下情况,对所配溶液浓度将有何影响?(填:偏低;偏高;无影响)
没有进行A操作__________;加蒸馏水时不慎超过了刻度__________;定容时俯视_________。
(6)若实验过程中出现如下情况如何处理?加蒸馏水时不慎超过了刻度_________;向容量瓶中转移溶液时(实验步骤②)不慎有液滴掉在容量瓶外面__________。
(1)配制250 mL 0.1 mol·L-1的盐酸溶液。?
应称量盐酸体积/mL | 应选用容量瓶的规格/mL | 除容量瓶外还需要的其他仪器 |
|
|
|
(2)容量瓶上除有刻度线外还应标有______________,在使用前必须检查容量瓶是否完好以及__________处是否漏水(填容量瓶的受检部位)。?
(3)配制时,其正确的操作顺序是(用字母表示,每个字母只能用一次)_________。?
A.用30 mL水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡?
B.用量筒准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30 mL),用玻璃棒慢慢搅动,使其混合均匀?
C.将已冷却的盐酸沿玻璃棒注入250 mL的容量瓶中?
D.将容量瓶盖紧,振荡,摇匀?
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切?
F.继续往容量瓶内小心加水,直到液面接近刻度2~3 cm处?
(4)操作A中,将洗涤液都移入容量瓶,其目的是__________________________。溶液注入容量瓶前需恢复到室温,这是因为______________________。?
(5)若出现如下情况,对所配溶液?浓度?将有何影响?(填:“偏低”“偏高”“无影响”)
没有进行A操作__________________;加蒸馏水时不慎超过了刻度____________________;定容时俯视__________________。?
(6)若实验过程中出现如下情况如何处理??
加蒸馏水时不慎超过了刻度______________;向容量瓶中转移溶液时(实验步骤②)不慎有液滴掉在容量瓶外面____________________。?
| |||||||||||||||||||||||||||
Ⅰ.用MnO2氧化密度为1.19 g·cm-3,溶质质量分数为36.5%的HCl溶液。反应的化学方程式为: 
(1)该盐酸的物质的量浓度为 mol/L。
(2)用双线桥法表示出该反应的电子转移方向和数目 。
(3)8.7gMnO2能使 molHCl被氧化。
Ⅱ.在一定体积的18 mol/L的浓硫酸中加入过量铜片,加热使之反应,若被还原
的硫酸为 0.9 mol。则浓硫酸的实际体积_________(填“大于”、“等于”或“小于”)100mL。若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为________________________________________________。
Ⅰ.用MnO2氧化密度为1.19 g·cm-3,溶质质量分数为36.5%的HCl溶液。反应的化学方程式为:
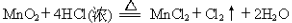
(1)该盐酸的物质的量浓度为 mol/L。
(2)用双线桥法表示出该反应的电子转移方向和数目 。
(3)8.7gMnO2能使 molHCl被氧化。
Ⅱ.在一定体积的18 mol/L的浓硫酸中加入过量铜片,加热使之反应,若被还原
的硫酸为 0.9 mol。则浓硫酸的实际体积_________(填“大于”、“等于”或“小于”)100mL。若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为________________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com