
题目列表(包括答案和解析)
利用所学化学反应原理,解决以下问题:
(1)某溶液含两种相同物质的量的溶质,且其中只存在OH一、H+、NH4+、Cl一四种离子,且c(NH4+)>c(Cl-)>c(OH-)>c(H+),则这两种溶质是________.
(2)0.1 mol·L-1的氨水与0.05 mol·L-1的稀硫酸等体积混合,用离子方程式表示混合后溶液的酸碱性:________.
(3)已知:Ksp(RX)=1.8×10-10,Ksp(RY)=1.5×10-16,Ksp(R2Z)=2.0×10-12,则难溶盐RX、RY和R2Z的饱和溶液中,R+浓度由大到小的顺序是________.
(4)向20 mL硫酸和盐酸的混合液中逐滴加入pH=13的Ba(OH)2溶液,生成BaSO4的量如下图所示,B点溶液的pH=7(假设体积可以直接相加),则c(HCl)=________mol·L-1.
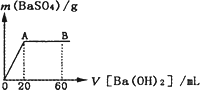
(5)在温度、容积相同的3个密闭容器中,按下表投入反应物,发生反应(H2(g)+I2(g)![]() 2HI(g) ΔH=-14.9 kJ·mol-1),在恒温、恒容条件下,测得反应达
2HI(g) ΔH=-14.9 kJ·mol-1),在恒温、恒容条件下,测得反应达
到平衡时的数据如下表:
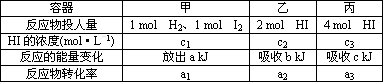
下列说法正确的是________.
A.α1+α2=1
B.2α2=α3
C.a+b=14.9
D.c1=c2=c3
某学生欲配制6.0 mol/L的H2SO4 1 000 mL,实验室有三种不同浓度的硫酸:
①480 mL 0.5 mol/L的硫酸;
②150 mL 25%的硫酸(ρ=1.18 g/mL);
③足量的18 mol/L的硫酸.
有三种规格的容量瓶:250 mL、500 mL、1 000 mL.老师要求把①②两种硫酸全部用完,不足的部分由③来补充.
请回答下列问题:
(1)实验所用25%的硫酸的物质的量浓度为________mol/L(保留1位小数).
(2)配制该硫酸溶液应选用容量瓶的规格为________mL.
(3)配制时,该同学的操作顺序如下,请将操作步骤B、D补充完整.
A.将①②两溶液全部在烧杯中混合均匀;
B.用量筒准确量取所需的18 mol/L的浓硫酸________mL,沿玻璃棒倒入上述混合液中.并用玻璃棒搅拌,使其混合均匀;
C.将混合均匀的硫酸沿玻璃棒注入所选的容量瓶中;
D.________________;
E.振荡,继续向容量瓶中加水,直到液面接近刻度线1~2 cm处;
F.改用胶头滴管加水,使溶液的凹液面恰好与刻度线相切;
G.将容量瓶盖紧,振荡,摇匀.
(4)如果省略操作D,对所配溶液浓度有何影响?________(填“偏大”、“偏小”或“无影响”).
(5)进行操作C前还需注意________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com