A、B均为无色盐溶液,B的焰色反应呈黄色,一定条件下A、B可以发生如图所示的物质之间的一系列变化:

若E为黄绿色气体,F为无色刺激性气味的气体,H不溶于稀硝酸.请填写下列空白.
(1)气体F的化学式为
SO2
SO2
,B中溶质的化学式为
Na2SO3
Na2SO3
.
(2)写出下列反应的离子方程式:C→E
;D+G→H
BaSO3+2H++SO42-=BaSO4↓+SO2↑+H2O
BaSO3+2H++SO42-=BaSO4↓+SO2↑+H2O
;
(3)试分析E和F按下列两种情况分别通入水中,所得溶液分别滴入几滴石蕊溶液的现象:
①E和F物质的量相等,现象为:
变红色
变红色
;原因为(用化学方程式表示)
Cl2+SO2+2H2O=H2SO4+2HCl
Cl2+SO2+2H2O=H2SO4+2HCl
.
②E和F物质的量不等,且E大于F,现象为:
先变红后褪色(或褪色)
先变红后褪色(或褪色)
;原因为(文字说明)
变红是因为溶液呈酸性,褪色是因为氯气过量生成次氯酸使溶液褪色
变红是因为溶液呈酸性,褪色是因为氯气过量生成次氯酸使溶液褪色
.
(4)向C的溶液中加入AgNO
3和KBr,当两种沉淀共存时,c(Br
-)/c(Cl
-)=
2.7×10-3
2.7×10-3
.
[已知:K
sp(AgBr)=5.4×10
-13,K
sp(AgCl)=2.0×10
-10].

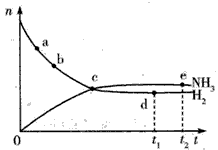
 2NH3(g)
2NH3(g) 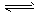 CO2(g) +H2(g) △H>0。
CO2(g) +H2(g) △H>0。 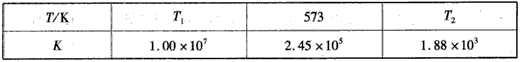
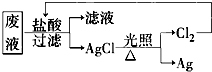
 国务院强调,“南水北调”工程必须坚持节水、治污和生态环境保护与工程建设相协调,以水资源合理配置为主线,把节水、治污、生态环境保护与调水作为一个完整的系统来分析的原则.在调水工程中,沿途工业污水的任意排放是造成水质恶化的最大隐患.检测某工厂废液中,含有大量的Mg2+、Al3+、Cu2+、Ag+.试分析回答下列问题:
国务院强调,“南水北调”工程必须坚持节水、治污和生态环境保护与工程建设相协调,以水资源合理配置为主线,把节水、治污、生态环境保护与调水作为一个完整的系统来分析的原则.在调水工程中,沿途工业污水的任意排放是造成水质恶化的最大隐患.检测某工厂废液中,含有大量的Mg2+、Al3+、Cu2+、Ag+.试分析回答下列问题: