
题目列表(包括答案和解析)
目前世界各国都在研究如何充分利用海洋资源,从海水中可得到大量粗盐.
(1)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、SO42-等杂质,必须精制后才能供电解使用.精制时,粗盐溶于水过滤后,还要加入的试剂分别为:①Na2CO3、②HCl(盐酸)、③BaCl2,这3种试剂添加的合理顺序是________(填序号).
(2)电解饱和食盐水常用离子膜电解槽和隔膜电解槽.电解槽中的阳极材料为________.在电解过程中,与电源正极相连的电极上所发生的化学方程式为________,与电源负极相连的电极附近,溶液pH将________(填“不变”、“升高”或“下降”).
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节能(电)30%以上.在这种工艺设计中,相关物料的传输与转化关系如图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过.图中X、Y分别是________、________(填化学式),分析比较图示中氢氧化钠质量分数a%________(填“大于”、“小于”或“等于”)b%.这样设计的主要节能(电)之处在于________、________(写出2处).
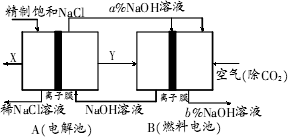
(4)氯气、烧碱是电解食盐水时按照固定的比率k(质量比)生成的产品.理论上k=________(要求计算表达式和结果).
| ||
| ||
| △ |
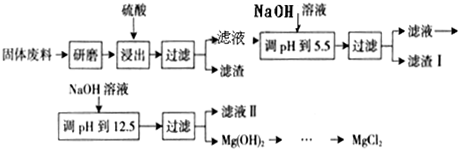
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| PH | 3.2 | 5.2 | 12.4 |
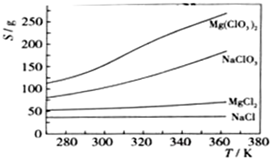
(1).
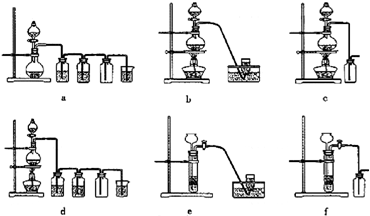
下列有关电化学的图示中,完全正确的是________
(2).
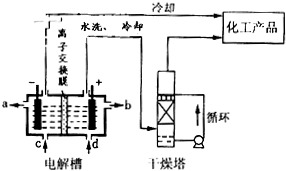
碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病.碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水.碘酸钾在酸性介质中可与碘化物作用生成单质碘.以碘为原料,通过电解制备碘酸钾的实验装置如图所示.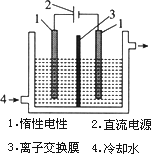
请回答下列问题:
a.碘是________(填颜色)固体物质,实验室常用________方法来分离提纯含有少量泥沙杂质的固体碘.
b.电解前,先将一定量的精制碘溶于过量氢氧化钾溶液,溶解时发生反应:3I2+6KOH![]() 5KI+KIO3+3H2O,将该溶液加入阳极区.另将氢氧化钾溶液加入阴极区,电解槽用水冷却.
5KI+KIO3+3H2O,将该溶液加入阳极区.另将氢氧化钾溶液加入阴极区,电解槽用水冷却.
电解时,阳极上发生反应的电极反应式为________,每生成1 mol KIO3,电路中通过的电子的物质的量为________.
c.电解过程中,为确定电解是否完成,需检验电解液中是否有I-.请设计一个检验电解液中是否有I-的简单实验方案,并按要求填写下表.
![]()
可供选择的试剂有淀粉溶液,稀硫酸,氯化钠溶液,酒精等.(用其中的一种或多种均可.)
d.电解完毕,从电解液中得到碘酸钾晶体的实验过程如下:
阳极电解液→①蒸发浓缩→②→③过滤→④洗涤→⑤→碘酸钾晶体
步骤②的操作名称是________,步骤⑤的操作名称是________.步骤④洗涤晶体的目的是________.
(12分)(1).下列有关电化学的图示中,完全正确的是
(2).碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病。碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水。碘酸钾在酸性介质中可与碘化物作用生成单质碘。以碘为原料,通过电解制备碘酸钾的实验装置如图所示。
请回答下列问题:
a、碘是 (填颜色)固体物质,实验室常用 方法来分离提纯含有少量泥沙杂质的固体碘。
b、电解前,先将一定量的精制碘溶于过量氢氧化钾溶
液,溶解时发生反应:3I2+6KOH==5KI+KIO3+3H2O,
将该溶液加入阳极区。另将氢氧化钾溶液加入阴极区,电解槽用水冷却。
电解时,阳极上发生反应的电极反应式为 ,每生成1mol KIO3,电路中通过的电子的物质的量为___________________。
c、电解过程中,为确定电解是否完成,需检验电解液中是否有I-。请设计一个检验
电解液中是否有I-的简单实验方案,并按要求填写下表。
可供选择的试剂有淀粉溶液,稀硫酸,氯化钠溶液,酒精等。(用其中的一种或多种均可。)
| 实验方法 | 实验现象及结论 |
|
|
|
d、电解完毕,从电解液中得到碘酸钾晶体的实验过程如下:
阳极电解液→①蒸发浓缩→②→③过滤→④洗涤→⑤→碘酸钾晶体
步骤②的操作名称是 ,步骤⑤的操作名称是 。步骤④洗涤
晶体的目的是 。
(12分)(1).下列有关电化学的图示中,完全正确的是 
(2).碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病。碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水。碘酸钾在酸性介质中可与碘化物作用生成单质碘。以碘为原料,通过电解制备碘酸钾的实验装置如图所示。
请回答下列问题:
a、碘是 (填颜色)固体物质,实验室常用 方法来分离提纯含有少量泥沙杂质的固体碘。
b、电解前,先将一定量的精制碘溶于过量氢氧化钾溶
液,溶解时发生反应:3I2+6KOH==5KI+KIO3+3H2O,
将该溶液加入阳极区。另将氢氧化钾溶液加入阴极区,电解槽用水冷却。
电解时,阳极上发生反应的电极反应式为 ,每生成1mol KIO3,电路中通过的电子的物质的量为___________________。
c、电解过程中,为确定电解是否完成,需检验电解液中是否有I-。请设计一个检验
电解液中是否有I-的简单实验方案,并按要求填写下表。
可供选择的试剂有淀粉溶液,稀硫酸,氯化钠溶液,酒精等。(用其中的一种或多种均可。)
| 实验方法 | 实验现象及结论 |
| | |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com