
题目列表(包括答案和解析)
| ||
| ||
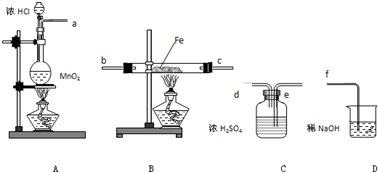

(1)若用Ⅰ制取氯气,b瓶加入的液体一般为 。在选取试剂正确且适量的前提下,反应开始后,当关闭活塞K时如若发现c中液面不明显上升,你分析可能的原因是 ,检查的简单方法是 。
(2)装置Ⅰ中b能防止多余气体逸散的原因是 。
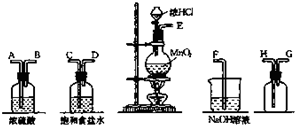
(3)欲用装置Ⅱ或装置Ⅲ代替Ⅰ中的b~c部分(选用液体相同),是否可行?说明理由。
装置Ⅱ是否可行 (填“是”或“否”),理由是 。
装置Ⅲ是否可行 (填“是”或“否”),理由是 。

图中:①为氯气发生装置;②的试管里盛有15 mL 30% KOH溶液。并置于热水浴中;③的试管里盛有15 mL 8% NaOH溶液。并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。
请填写下列空白:
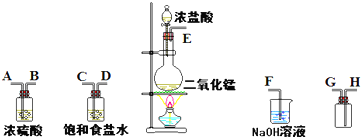
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过_____________(填写仪器名称)向烧瓶中加入适量的浓盐酸。实验时为了除去氯气中的氯化氢气体,可在①与②之间安装盛有_____________(填写下列编号字母)的净化装置。
A.碱石灰 B.饱和食盐水
C.浓硫酸 D.饱和碳酸氢钠溶液
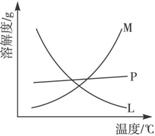
(2)比较制取氯酸钾和次氯酸钠的条件。二者的差异是______。反应完毕经冷却后,②的试管中有大量晶体析出。下图中符合该晶体溶解度曲线的是______(填写编号字母);从②的试管中分离出该晶体的方法是______________(填写实验操作名称 )。
(3)本实验中制取次氯酸钠的离子方程式是:__________________________。
(4)实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白:
实验现象 | 原因 |
溶液最初从紫色逐渐变为_____________色 | 氯气与水反应生成的H+使石蕊变色 |
随后溶液逐渐变为无色 | _____________ |
然后溶液从无色逐渐变为_____________色 | _____________ |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com