
题目列表(包括答案和解析)
(2)在一体积为
CO(g)+H2O(g) ![]() CO2(g)+H2(g)+Q(Q>0)
CO2(g)+H2(g)+Q(Q>0)
CO和H2O浓度变化如下图,则0—4 min间平均反应速率v(CO)=____________ mol·L-1·min-1。

t ℃时物质浓度(mol·L-1)的变化
时间/min | CO | H2O | CO2 | H2 |
0 | 0.200 | 0.300 | 0 | 0 |
2 | 0.138 | 0.238 | 0.062 | 0.062 |
3 | c1 | c2 | c3 | c3 |
4 | c1 | c2 | c3 | c3 |
5 | 0.116 | 0.216 | 0.084 |
|
6 | 0.096 | 0.266 | 0.104 |
|
(3)t ℃(高于850 ℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表。
①表中3—4 min之间反应处于_________状态;c1数值_________0.08 mol·L-1(填“大于”“小于”或“等于”)。
②反应在4—5 min间,平衡向逆方向移动,可能的原因是___________(单选),表中5—6 min之间数值发生变化,可能的原因是___________(单选)。
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增大氢气浓度
①该学生的操作是__________(填“正确的”或“错误的”),其理由是___________________。
②如不正确请说明理由,同时请分析是否一定有误差?答_____________________。
③若用此法分别测定[H+]相等的盐酸和醋酸溶液的pH,误差较大的是_________________,原因是_____________________________________________。
(2)若以铁棒、碳棒、导线和氯化铁溶液为用品设计原电池。
负极材料为_______________,电极反应式为_______________;
正极材料为_______________,电极反应式为_______________;
电池总反应式为______________________________________________________。
(3)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热。已知:0.4 mol液态肼与足量的液态双氧水反应,生成氮气和水蒸气,放出256.652 kJ的热量。
①反应的热化学方程式为__________________。
②又已知H2O(l)![]() H2O(g) ΔH=+44 kJ·mol-1,则
H2O(g) ΔH=+44 kJ·mol-1,则
③此反应用于火箭推进,除释放大量热和快速产生大量气体外还有一个很大的优点是_________。
(1)该有机物的结构简式和名称。
(2)该有机物的两种主要用途。
4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g);ΔH=-905 kJ·mol-1
4NO(g)+6H2O(g);ΔH=-905 kJ·mol-1
2H2(g)+O2(g)![]() 2H2O;ΔH=-483.6 kJ·mol-1
2H2O;ΔH=-483.6 kJ·mol-1
则N2(g)+3H2(g)![]() 2NH3(g)的ΔH=________。
2NH3(g)的ΔH=________。
(2)工业上在一定温度下,将一定量的N2和H2通入到体积为
①增大压强②增大反应物的浓度③使用催化剂④降低温度
(3)当化学反应N2(g)+2H2(g) ![]() 2NH3(g)达到平衡后改变某些条件(不改变N2、H2和NH3的用量),反应速率与反应时间的关系如下图,其中表示平衡混合物中NH3的含量最高的一段时间是___________________。当温度为T ℃时,将
2NH3(g)达到平衡后改变某些条件(不改变N2、H2和NH3的用量),反应速率与反应时间的关系如下图,其中表示平衡混合物中NH3的含量最高的一段时间是___________________。当温度为T ℃时,将

(4)合成氨的原料氢气是一种新型的绿色能源,具有广阔的发展前景。现用氢氧燃料电池进行下图所示实验:

①请写出氢氧燃料电池中的电极反应式:
负极:____________________________________________________________;
正极:____________________________________________________________。
②上图装置中,某一铜电极的质量减轻了
1 mol的某有机物甲在O2中充分燃烧,可得到相同条件下等体积的CO2和H2O(g),并消耗112L(标准状况)O2;又知甲的相对分子质量小于100,1 mol甲在酸性条件下可水解生成1 mol乙和1 mol丙,且丙通过一定途径可转化为乙。
(1)甲的分子式为 。
(2)与甲分子式、所属物质类别都相同的有机物的同分异构体有 种(不含甲)。
|
|
|
②RCH—CHR1 → RCHO+R1CHO
| |
OH OH
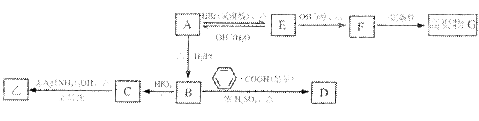 A与甲为同分异构体,且A中含有碳氧双键,B只生成C,与A相关的反应如下:
A与甲为同分异构体,且A中含有碳氧双键,B只生成C,与A相关的反应如下:
(3)写出E→F的反应类型: 。
(4)写出A、G的结构简式:A 、G 。
(5)写出下列转化的反应化学方程式:
B→D ;
C在反应条件为:①下发生反应的化学方程式为 。
(6)A在空气中久置,可转化为相对分子质量为86的化合物H,H的一氯代物只有一种,写出H的结构简式: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com