
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
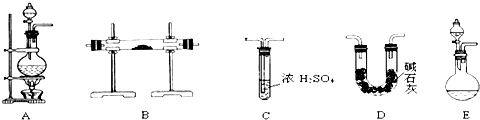
| NaOHШмвК |
ТСУОКЯН№вбГЩЮЊТжДЌжЦдьЁЂЛЏЙЄЩњВњЕШаавЕЕФживЊВФСЯЁЃбаОПадбЇЯАаЁзщЮЊВтЖЈФГКЌУО3ЃЅвЛ5ЃЅЕФТСУОКЯН№(ВЛКЌЦфЫќдЊЫи)жаУОЕФжЪСПЗжЪ§ЃЌЩшМЦвдЯТЪЕбщЗНАИНјааЬНОПЁЃЬюаДЯТСаПеАзЁЃ
ЃлЪЕбщЗНАИЃн ТСУОКЯН№ЗлФЉ![]() ВтЖЈЪЃгрЙЬЬхжЪСП
ВтЖЈЪЃгрЙЬЬхжЪСП
ЃлЪЕбщВНжшЃн
ВНжш1ЃКГЦШЁ5ЃЎ4gТСУОКЯН№ЗлФЉбљЦЗЃЌЭЖШыVmL 2ЃЎ0molЁЄLЁЊ1NaOHШмвКжаЃЌГфЗжЗДгІЁЃ
ВНжш2ЃКЙ§ТЫЁЂЯДЕгЁЂИЩдяЁЂГЦСПЙЬЬхЁЃ
[НЛСїгыЬжТл]
(1) ЪЕбщжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЪЧ ЃЛ
(2)ВЮгыЗДгІЕФNaOHШмвКЕФЬхЛ§VЁн ЃЛ
(3)ВНжш2жаЃЌШчЙћОСНДЮЙ§ТЫТЫвКШдЛызЧЃЌдђдвђПЩФмЪЧ_________(жЛЬювЛЕу)ЃЛ
(4)ВНжш2жаЃЌШєЮДЯДЕгЙЬЬхЃЌВтЕУУОЕФжЪСПЗжЪ§НЋ (ЬюЁАЦЋИпЁБЛђЁАЦЋЕЭЁБ)ЁЃ
[ЪЕбщЭиеЙ] ЧыФуСэЩшМЦвЛИіЪЕбщЗНАИ(гУЩЯЪіЗНАИЕФЪдМС)ЃЌВтЖЈИУТСУОКЯН№жаУОЕФжЪСПЗжЪ§ЁЃ
вЊЧѓЃКДгЯТЭМжаЬєбЁЫљашЕФвЧЦїЃЌЛГіИУЗНАИЕФЪЕбщзАжУМђЭМЃЈЬэМгБивЊЕФШћзгЁЂВЃСЇЕМЙмЁЂНКЦЄЙмЃЌЙЬЖЈзАжУВЛгУЛЃЉЃЌВЂБъУїЫљгУЪдМС.


(12Зж) Ђё.ЯТЭМБэЪО4ИіЬМдзгЯрЛЅНсКЯЕФЗНЪНЁЃаЁЧђБэЪОЬМдзгЃЌаЁЙїБэЪОЛЏбЇМќЃЌМйШчЬМдзгЩЯЦфгрЕФЛЏбЇМќЖМЪЧгыЧтНсКЯЁЃ

ЃЈ1ЃЉЭМжаЪєгкЭщЬўЕФЪЧ ЃЈЬюБрКХЃЉЪєгкЯЉЬўЕФЪЧ ЃЌЃЈЬюБрКХЃЉ
ЃЈ2ЃЉЩЯЭМжагыBЛЅЮЊЭЌЗжвьЙЙЬхЕЋВЛЪєгкЭЌжжРрЕФЮяжЪЕФЪЧЃК ЁЃЃЈЬюБрКХЃЉ
ЂђЃЎПЮБОЁАНЛСї•баЬжЁБРИФПгаетбљвЛзщЪ§ОнЃКЦЦЛЕ1molЧтЦјжаЕФЛЏбЇМќашвЊЮќЪе436kJФмСПЃЛЦЦЛЕ1/2molбѕЦјжаЕФЛЏбЇМќашвЊЮќЪе249kJЕФФмСПЃЛаЮГЩЫЎЗжзгжа1 mol HЁЊOМќФмЙЛЪЭЗХ463kJФмСПЁЃ
ЯТЭМБэЪОЧтЦјКЭбѕЦјЗДгІЙ§ГЬжаФмСПЕФБфЛЏЃЌЧыНЋЭМжаЂйЁЂЂкЁЂЂлЕФФмСПБфЛЏЕФЪ§жЕЃЌЬюдкЯТБпЕФКсЯпЩЯЁЃ

Ђй kJ Ђк kJ Ђл kJ
IЃЎЯТЭМБэЪО4ИіЬМдзгЯрЛЅНсКЯЕФЗНЪНЁЃаЁЧђБэЪОЬМдзгЃЌаЁЙїБэЪОЛЏбЇМќЃЌМйШчЬМдзгЩЯЦфгрЕФЛЏбЇМќЖМЪЧгыЧтНсКЯЁЃ
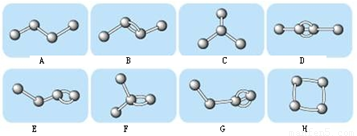
ЃЈ1ЃЉЭМжаЪєгкЭщЬўЕФЪЧ ЃЈЬюБрКХЃЉЃЛЪєгкЯЉЬўЕФЪЧ ЃЈЬюБрКХЃЉЃЛ
ЃЈ2ЃЉЩЯЭМжагыBЛЅЮЊЭЌЗжвьЙЙЬхЕЋВЛЪєгкЭЌжжРрЕФЮяжЪЕФЪЧЃК ЁЃЃЈЬюБрКХЃЉ
IIЃЎПЮБОЁАНЛСї•баЬжЁБРИФПгаетбљвЛзщЪ§ОнЃКЦЦЛЕ1molЧтЦјжаЕФЛЏбЇМќашвЊЮќЪе436kJФмСПЃЛЦЦЛЕ1/2molбѕЦјжаЕФЛЏбЇМќашвЊЮќЪе249kJЕФФмСПЃЛаЮГЩЫЎЗжзгжа1 mol HЁЊOМќФмЙЛЪЭЗХ463kJФмСПЁЃ
ЯТЭМБэЪОЧтЦјКЭбѕЦјЗДгІЙ§ГЬжаФмСПЕФБфЛЏЃЌЧыНЋЭМжаЂйЁЂЂкЁЂЂлЕФФмСПБфЛЏЕФЪ§жЕЃЌЬюдкЯТБпЕФКсЯпЩЯЁЃ
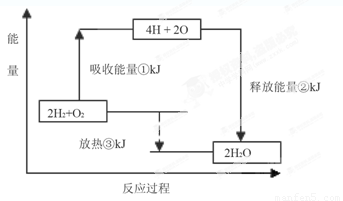
Ђй kJЃЛЂк kJЃЛЂл kJЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com