
题目列表(包括答案和解析)
已知化学反应2C(s)+O2(g) ![]() 2CO(g)、2CO(g)+O2(g)
2CO(g)、2CO(g)+O2(g) ![]() 2CO2(g)都是放热反应,据此判断,下列说法中不正确的是
2CO2(g)都是放热反应,据此判断,下列说法中不正确的是
A.12gC所具有的能量一定高于28gCO所具有的能量
B.56gCO和32gO2所具有的总能量大于44gCO2所具有的总能量
C.12gC和32gO2所具有的总能量大于44gCO2所具有的总能量
D.将一定质量的C燃烧,生成CO2比生成CO时放出的热量多
I.已知:TiO2(s)+2Cl2(g)=TiCl4(l)+O2(g) △H=+140kJ·mol-1
2C(s)+O2(g)=2CO(g) △H=-221kJ·mol-1
写出TiO2和焦炭、氯气反应生成液态TiCl4和CO气体的热化学方程式: 。
II.将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s) 2NH3(g)+CO2(g)
2NH3(g)+CO2(g)
则可以判断该分解反应已经达到平衡状态的是 。
A.2v正(NH3)=v逆(CO2) B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变 D.密闭容器中氨气的体积分数不变
III.以丙烷为燃料制作新型燃料电池,电解质是熔融碳酸盐。电池的一极通入O2和CO2,电极反应式为:O2+2CO2+4e-=2CO32-;另一极通入丙烷,电极反应式为 ;放电时,CO32-移向电池的 (填“正”或“负”)极。
IV.如图装置所示,C、D、E、F都是惰性电极,甲、乙中溶液的体积和物质的量浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。

⑴若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为 。
⑵现用丙装置作“铜的电解精炼”,则H应该是 。(填“纯铜”或“粗铜”)。
⑶上图甲装置电解CuSO4溶液一段时间后,向所得溶液中加入0.2mol Cu(OH)2后,恰好使溶液恢复到电解前的浓度。则乙装置中,若不考虑Cl2的溶解及与碱的反应,此装置共产生气体 L(标准状况)。
 2NH3(g)+CO2(g)
2NH3(g)+CO2(g)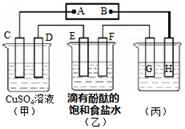
已知化学反应2C(s)+O2(g) ="==" 2CO(g)、2CO(g)+O2(g) ===2CO2(g)都是放热反应。据此判断,下列说法不正确的是(其他条件相同)( )。
| A.12 g C所具有的能量一定高于28 g CO所具有的能量 |
| B.56 g CO和32 g O2所具有的总能量大于88 g CO2所具有的总能量 |
| C.12 g C和32 g O2所具有的总能量大于44 g CO2所具有的总能量 |
| D.将一定质量的C燃烧,生成CO2比生成CO时放出的热量多 |
|
已知化学反应2C(s)+O2(g) | |
| [ ] | |
A. |
12 g C所具有的能量一定高于28 g CO所具有的能量 |
B. |
56 g CO和32 g O2所具有的总能量大于88 g CO2所具有的总能量 |
C. |
12 g C和32 g O2所具有的总能量大于44 g CO2所具有的总能量 |
D. |
将一定质量的C燃烧,生成CO2比生成CO时放出的热量多 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com