
题目列表(包括答案和解析)
| A.相同条件下反应2SO2(g)+O2(g)?2SO3(g)与4SO2(g)+2O2(g)?4SO3(g)的△H相等 |
| B.甲烷的标准燃烧热为-890.3kJ/mol,则甲烷燃烧的热化学方程式可以表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3kJ/mol |
| C.在一定温度和压强下,将0.5molN2和1.5molH2置于密闭容器中充分反应生成NH3(g),放出热量19.3kJ,则其热化学方程式为N2(g)+3H2(g)?2 NH3(g)△H=-38.6kJ/mol |
| D.一定条件下2SO2(g)+O2(g)?2SO3(g)△H1 2SO2(g)+O2(g)?2SO3(l)△H2 则△H1>△H2 |
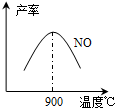 工业合成氨与制备硝酸一般可连续生产,流程如下:
工业合成氨与制备硝酸一般可连续生产,流程如下: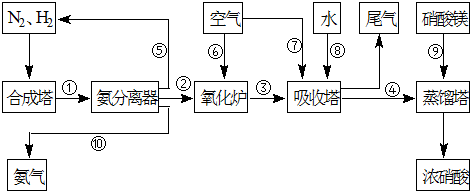
| T/℃ | T1 | 300 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com