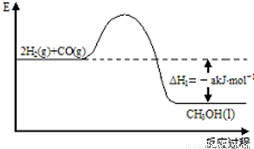
能源是人类生存和发展的重要支柱.研究和有效地开发新能源在能源紧缺的今天具有重要的理论意义.已知H
2与CO反应生成CH
3OH的过程如图所示:CO的燃烧热△H
2=-bkJ?mol
-1,CH
3OH的燃烧热△H
3=-ckJ?mol
-1.请根据以上信息,回答下列有关问题:
(1)CH
3OH燃烧的热化学反应方程式为
2CH3OH(l)+3O2(g)→2CO2(g)+4H2O(l)△H=-2ckJ?mol-1
2CH3OH(l)+3O2(g)→2CO2(g)+4H2O(l)△H=-2ckJ?mol-1
.
(2)H
2的燃烧热为
.
(3)一些化学键键能如下:C≡O为d kJ/mol;O=O为ekJ/mol;C=O为fkJ/mol.则由以上数据有b=
(用d、e、f的代数式表示).
(4)H
2和CO的混合气体nmol,充分燃烧共放出QkJ热量,则混合气体中H
2和CO的物质的量之比为
(2bn-2Q):(bn-an-cn+2Q)
(2bn-2Q):(bn-an-cn+2Q)
.
(5)CO与O
2可以组成新型燃料电池,若该电池以Pt为电极,以KOH为电解质溶液,写出该燃料电池的负极反应式
CO-2e-+4OH-=CO32-+2H2O
CO-2e-+4OH-=CO32-+2H2O
.

 能源是人类生存和发展的重要支柱.研究和有效地开发新能源在能源紧缺的今天具有重要的理论意义.已知H2与CO反应生成CH3OH的过程如图所示:CO的燃烧热△H2=-bkJ?mol-1,CH3OH的燃烧热△H3=-ckJ?mol-1.请根据以上信息,回答下列有关问题:
能源是人类生存和发展的重要支柱.研究和有效地开发新能源在能源紧缺的今天具有重要的理论意义.已知H2与CO反应生成CH3OH的过程如图所示:CO的燃烧热△H2=-bkJ?mol-1,CH3OH的燃烧热△H3=-ckJ?mol-1.请根据以上信息,回答下列有关问题: