
题目列表(包括答案和解析)

| ||
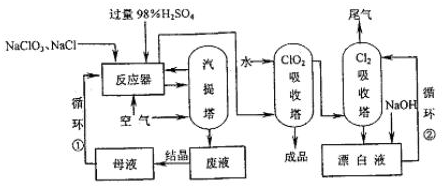
(1)工业上用NaCl还原NaClO3生产ClO2的工艺流程如下图所示:

①反应器中发生反应的化学方程式为:
2NaClO3+2NaCl+2H2SO4![]() 2ClO2↑+Cl2↑+2Na2SO4+2H2O
2ClO2↑+Cl2↑+2Na2SO4+2H2O
生产中将NaClO3和NaCl按物质的量之比1∶1.05的混合水溶液加入反应器,NaCl稍过量的目的是___________________________________________________________________。
②反应器中生成的ClO2和Cl2由通入空气驱出进入ClO2吸收塔,产生的混合液进入汽提塔,汽提塔排出的废液成分主要是______________(填化学式,下同)。
③以上生产流程中循环②循环利用的物质是______________。
④为提高ClO2的产量,可用亚氯酸钠(NaClO2)与反应器中的Cl2反应生成ClO2,该反应的化学方程式为________________________________________________。尾气中的Cl2可用SO2水溶液吸收,该反应的化学方程式为_____________________________________________。
(2)用阳离子交换膜分隔的电解池电解
A.电解时电子流向为:电源负极→导线→阴极,阳极→导线→电源正极
B.在电解过程中,Na+向阳极移动,![]() 向阴极移动
向阴极移动
C.在电解过程中阳极周围的pH基本不变
D.电解的离子方程式可表示为:2![]() +2H2O
+2H2O![]() 2ClO2↑+H2↑+2OH-
2ClO2↑+H2↑+2OH-
 2ClO2↑+H2↑+2OH-.
2ClO2↑+H2↑+2OH-.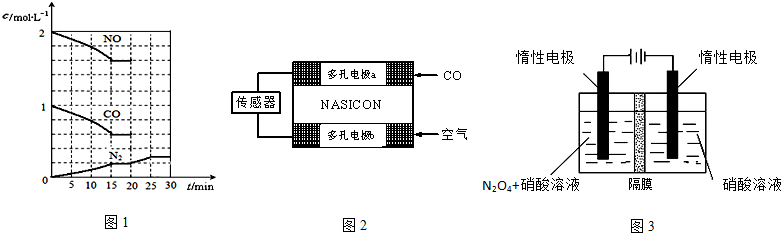
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com