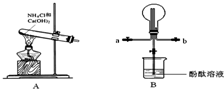
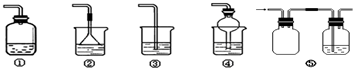
某小组利用如图装置制备氨气,并探究氨气的性质(部分仪器略去).请回答:

(1)实验室制备氨气的化学方程式为
2NH
4Cl+Ca(OH)
2CaCl
2+2NH
3+2H
2O
2NH
4Cl+Ca(OH)
2CaCl
2+2NH
3+2H
2O
.
(2)用B装置收集氨气时,请你选择氨气的进气口
a
a
(填“a”或“b”).
(3)B装置中烧瓶已收集满氨气,若使之形成喷泉,你的操作方法是
打开下方止水夹,用手(或热毛巾)捂热烧瓶,使氨气受热膨胀,赶出玻璃管内空气,氨气与水接触形成喷泉
打开下方止水夹,用手(或热毛巾)捂热烧瓶,使氨气受热膨胀,赶出玻璃管内空气,氨气与水接触形成喷泉
.若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气具有的性质是
极易溶于水,与水反应生成碱
极易溶于水,与水反应生成碱
.
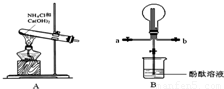
(4)为防止环境污染,以下装置(盛放的液体均为水)可用于吸收多余氨气的是
②④⑤
②④⑤
(填序号).

(5)氨气在催化剂作用下并且加热时会被空气氧化,这是工业制硝酸的第一步反应,写出该反应的化学方程式
.
(6)氨气和氯气在常温下可快速反应生成氮气:2NH
3+3Cl
2=N
2+6HCl.该反应可用于检验化工生产中氯气是否泄漏.因为氯气有少量泄漏,用氨气检验时会有明显现象,此过程中发生反应的Cl
2和NH
3的体积比范围为
小于1.5
小于1.5
.