
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
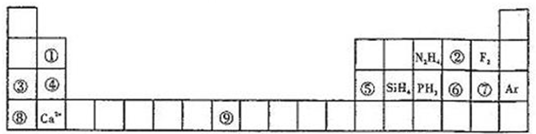
ЯюФП | ЭЌжмЦк(зѓЁњгв) | ЭЌжїзх(ЩЯЁњЯТ) | |
дзгНсЙЙ | КЫЕчКЩЪ§ | ж№НЅ__________ | ж№НЅ__________ |
ЕчзгВуЪ§ | __________ | ж№НЅ__________ | |
дзгАыОЖ | ж№НЅ__________ | ж№НЅ__________ | |
аджЪ | ЛЏКЯМл | зюИпе§МлгЩ__________ЃЌИКМлЪ§=__________ | зюИпе§МлЁЂИКМлЪ§ЯрЭЌзюИпе§Мл=__________ |
дЊЫидзгЕФЕУЕчзгФмСІКЭЪЇЕчзгФмСІ | ЪЇЕчзгФмСІж№НЅ__________ ЕУЕчзгФмСІж№НЅ__________ | ЪЇЕчзгФмСІж№НЅ__________ ЕУЕчзгФмСІж№НЅ__________ | |
ЕЅжЪЕФбѕЛЏадЁЂЛЙдад | ЛЙдад__________ бѕЛЏад__________ | бѕЛЏад__________ ЛЙдад__________ | |
зюИпМлбѕЛЏЮяЖдгІЕФЫЎЛЏЮяЕФЫсМюад | Мюад__________ Ысад__________ | Ысад__________ Мюад__________ | |
ЦјЬЌЧтЛЏЮяЮШЖЈад | __________ | __________ | |
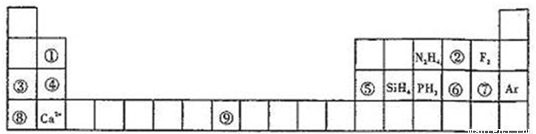
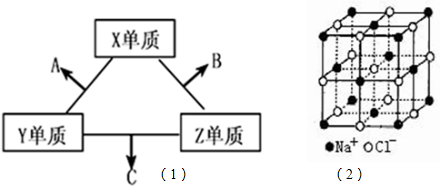

ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com