(1 5分)
原子序数依次递增的X、Y、Z、W是周期表中前30号元素,其中只有X、Y同周期。已知X的最外层电子数是其内层电子数的2倍;X与Y形成的常见化合物之一常被用于高炉炼铁;Z与X同主族,其单质在同周期元素形成的单质中熔点最高;W原子M能层为全充满状态,且核外的未成对电子只有一个。回答下列问题:
(1)X能形成多种常见单质,在熔点最低的单质中,每个分子周围紧邻的分子数为 ;在熔点最高的两种单质中,X的杂化方式分别为 、 。
(2)X、Y分别与H形成的化学键的极性关系为X—H Y—H,键能关系为
X—H __Y—H(填“<”、“>”或“=”)。
(3)+1价气态基态阳离子再失去一个电子形成+2价气态基态阳离子所需要的能量称为第二电离能I2,依次还有I3、I4、I5…,推测Z元素的电离能突增应出现在第 电离能。
(4)短周期元素中有一种元素与Z元素位于不同周期的相邻主族,且性质与Z十分相似,由该元素形成的单质属于 晶体。
(5)W的价电子排布图为 ;W的基态原子有 种形状不同的原子轨道,W基态原子有 种形状不同的原子轨道;W单质中W原子的配位数为 ;下图 表示的是W晶体中微粒的堆积方式(填甲、乙或丙);工业冶炼W的单质有两种常见方法,写出火法炼W的化学方程式 。
(6)向W的硫酸盐溶液中逐滴滴加氨水至过量,最终形成的化合物中含 、 键(填化学键类型,任写两种即可)。



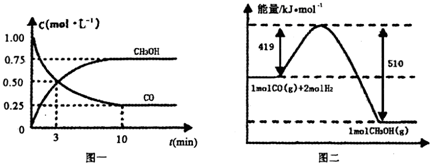
 “低碳循环”引起各国的高度重视,已知煤、甲烷等可以与水蒸气反应生成以CO和H2为主的合成气,合成气有广泛应用.试回答下列问题:
“低碳循环”引起各国的高度重视,已知煤、甲烷等可以与水蒸气反应生成以CO和H2为主的合成气,合成气有广泛应用.试回答下列问题: