
题目列表(包括答案和解析)
实验室制取乙烯常因温度过高生成少量SO2,有人设计了下列实验以验证上述混合气体中含有乙烯和SO2。
(1)如图5-4,A、B、C、D装置中可盛放的试剂是(填序号):
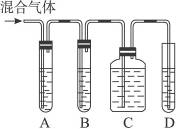
图5-4
A. ________________;B. ________________;C. ________________;D. ________________。
①品红溶液 ②NaOH溶液 ③溴水 ④KMnO4酸性溶液
(2)能说明SO2气体存在的现象是___________________________。
(3)使用装置B的目的是__________________。
(4)使用装置C的目的是__________________。
(5)确定含有乙烯的现象是__________________。




 化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:| c(CH3OH) |
| c(CO)c2(H2) |
| c(CH3OH) |
| c(CO)c2(H2) |
| 2nB |
| 3tB |
| 2nB |
| 3tB |
| O | 2- 3 |




湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com