
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
| |||||||||||
| |||||||||||
|
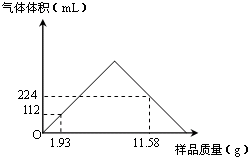
дк20ЁцЪБЃЌНЋ10 gФІЖћжЪСПЮЊM(A)(g/mol)ЕФAЮяжЪЭЖШы90 gЫЎжаЃЌИеКУЭъШЋШмНтЃЌаЮГЩЕФШмвКЮЊБЅКЭШмвК(МйЩшШмвКЕФУмЖШЮЊ1 g/mL)ЃЌдђЯТСаЫЕЗЈжае§ШЗЕФЪЧ | |
| [ЁЁЁЁ] | |
AЃЎ |
20ЁцЪБЃЌAЕФШмНтЖШвЛЖЈЪЧ100/9 g |
BЃЎ |
20ЁцЪБЃЌAЕФШмНтЖШПЩФмЪЧ10 g |
CЃЎ |
аЮГЩЕФБЅКЭШмвКЕФШмжЪжЪСПЗжЪ§вЛЖЈЮЊ10ЃЅ |
DЃЎ |
аЮГЩЕФБЅКЭШмвКЕФЮяжЪЕФСПХЈЖШвЛЖЈЮЊ100/M(A)mol/L |
 КЌБЕЛЏКЯЮядкЪЕбщЪвКЭЙЄвЕЩњВњжаЖМгаЙуЗКЕФгУЭОЃЎ
КЌБЕЛЏКЯЮядкЪЕбщЪвКЭЙЄвЕЩњВњжаЖМгаЙуЗКЕФгУЭОЃЎ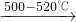 2BaO2ЃЎЯжга16.0ЖжЕФбѕЛЏБЕдкзуСПЕФбѕЦјжаМгШШЗДгІКѓЃЌЙЬЬхЕФжЪСПБфЮЊ17.6ЖжЃЎФЧУДЪЕМЪВЮМгЗДгІЕФбѕЛЏБЕЕФжЪСПЮЊ______ЖжЃЎ
2BaO2ЃЎЯжга16.0ЖжЕФбѕЛЏБЕдкзуСПЕФбѕЦјжаМгШШЗДгІКѓЃЌЙЬЬхЕФжЪСПБфЮЊ17.6ЖжЃЎФЧУДЪЕМЪВЮМгЗДгІЕФбѕЛЏБЕЕФжЪСПЮЊ______ЖжЃЎ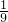 ЃЌЧѓИУЗДгІЬѕМўЯТЛьКЯЦјЬхЕФЦНОљЪНСПЃП
ЃЌЧѓИУЗДгІЬѕМўЯТЛьКЯЦјЬхЕФЦНОљЪНСПЃП(1)ЕчНтЪБЫљШЁБЅКЭТШЛЏФЦШмвКЕФжЪСПЁЃ
(2)ЕчНтКѓШмвКжаЧтбѕЛЏФЦЕФЮяжЪЕФСПХЈЖШЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com