
题目列表(包括答案和解析)
完成下列问题:
(1)写出溶液A中电解质的化学式。
(2)写出上述滴定反应的离子方程式。
(3)已知用于滴定的PbI2的浓度为0.009 854 mol·L-1,滴定完成时消耗掉PbI2溶液21.03 mL,则共析出金属铅多少毫克?(铅的相对原子质量为207.2,钠的相对原子质量为22.99)
物质的转化关系如图所示(有的反应可能在水溶液中进行)。其中甲为淡黄色固体化合物,乙为金属单质,G为酸,乙在G的浓溶液中发生钝化,用两根玻璃棒分别蘸取化合物A、G的浓溶液并使它们接近,有大量白烟生成。请回答下列问题: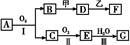
(1)写出甲的电子式: 。
(2)写出反应Ⅰ的化学方程式: 。
(3)A溶于水得到溶液X,在25 ℃下,将a mol·L-1的X与b mol·L-1的G溶液等体积混合,溶液显中性,则所得溶液中离子浓度由大到小的顺序为 ,
用含a和b的代数式表示出该混合溶液中X的电离平衡常数 。
(4)工业上采用的一种污水处理方法是:保持污水的pH在5.0~6.0之间,通过如图装置处理污水。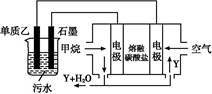
①电解池阳极发生了两个电极反应,其中一个反应生成一种无色气体,则阳极的电极反应式分别是:Ⅰ. ;Ⅱ. 。
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分Y物质参加循环(见上图)。Y物质的化学式是 。
物质的转化关系如图所示(有的反应可能在水溶液中进行)。其中甲为淡黄色固体化合物,乙为金属单质,G为酸,乙在G的浓溶液中发生钝化,用两根玻璃棒分别蘸取化合物A、G的浓溶液并使它们接近,有大量白烟生成。请回答下列问题:

(1)写出甲的电子式: 。
(2)写出反应Ⅰ的化学方程式: 。
(3)A溶于水得到溶液X,在25 ℃下,将a mol·L-1的X与b mol·L-1的G溶液等体积混合,溶液显中性,则所得溶液中离子浓度由大到小的顺序为 ,
用含a和b的代数式表示出该混合溶液中X的电离平衡常数 。
(4)工业上采用的一种污水处理方法是:保持污水的pH在5.0~6.0之间,通过如图装置处理污水。

①电解池阳极发生了两个电极反应,其中一个反应生成一种无色气体,则阳极的电极反应式分别是:Ⅰ. ;Ⅱ. 。
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分Y物质参加循环(见上图)。Y物质的化学式是 。


(10分)质量为34 g的NH3其物质的量是 mol,在标准状况下的体积约为 L 。0.1 mol H2S中有约 个氢原子;相同质量的NH3和H2S中分子个数比为 。配制100 mL浓度为1 mol·L-1的稀硫酸,需要用98%密度为1.84 g/cm3的浓硫酸 mL。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com