
题目列表(包括答案和解析)
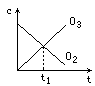
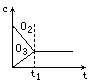
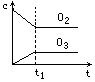
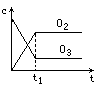
将5mol·L-1的O2在高温下放电,经时间t1后,建立了3O2![]() 2O3的平衡体系,测知氧气的转化率为20%,则如图中所示图像正确的是
2O3的平衡体系,测知氧气的转化率为20%,则如图中所示图像正确的是
[ ]
《环境空气质量标准》中,有害气体的浓度常用标准状况下,每立方米气体中含有害气体的毫克值(mg/m3)来表示,对CO的浓度限值规定为:
一、二级标准:4.00,三级标准:6.00 。一环保检测中心对采集的0.02m3(标况)某区域空气样品中所含CO的浓度进行测定,其方法和实验步骤如下:
① 首先将空气样品通过盛有I2O5固体的加热管,反应生成CO2和I2(不考虑其他气体的反应);
② 用30.0mL 5.00×10-5mol·L-1过量的硫代硫酸钠溶液完全吸收反应所产生的碘,发生的反应为:I2+2S2O32-=2I-+S4O62-
③ 将②反应后溶液取出1/2,放入锥形瓶中,加入几滴指示剂,用1.00×10-5mol·L-1的标准碘溶液进行滴定,滴定至终点,实验记录如下:

(1) 写出中反应的化学方程式:
(2) 计算该空气样品中CO的浓度,并说明符合几级标准。
《环境空气质量标准》中,有害气体的浓度常用标准状况下,每立方米气体中含有害气体的毫克值(mg/m3)来表示,对CO的浓度限值规定为:一级、二级标准:4.00,三级标准:6.00 。某环保检测中心对采集的0.02m3(标况)某区域空气样品中所含CO的浓度进行测定,其方法和实验步骤如下:
① 首先将空气样品通过盛有I2O5固体的加热管,反应生成CO2和I2
(不考虑其他气体的反应);
② 用30.0mL 5.00×10-5mol?L-1过量的硫代硫酸钠溶液完全吸收反应所产生的碘,发生的反应为:I2+2S2O32-=2I-+S4O62-
③ 将②反应后溶液取出1/2,放入锥形瓶中,加入几滴指示剂,用1.00×10-5mol?L-1的标准碘溶液进行滴定,滴定至终点,实验记录如下:
| 滴定次数 | 1.00×10-3mol?L-1标准碘溶液体积/mL | |
| 滴定前刻度 | 滴定后刻度 | |
| 1 | 0.00 | 10.01 |
| 2 | 1.21 | 11.20 |
(1)写出①中反应的化学方程式:
(2)计算该空气样品中CO的浓度,并说明符合几级标准。
(11分)某学生需要用0.5mol·L-1的NaCl溶液80mL ,并到实验室进行配制。试回答下列各题。
(1)经计算,应该用托盘天平称取NaCl固体_________g。
(2)若用NaCl固体配制溶液,需使用的玻璃仪器有_________________ ____________
(3)配制过程有以下操作:A.移液,B.称量,C.洗涤,D.定容,E.溶解,F.摇匀。其正确的操作顺序应是_______________________ (填序号)。
(4)下列操作会导致所得溶液浓度偏低的是______________(填序号)。
A.定容时仰视容量瓶刻度线
B.定容时俯视容量瓶刻度线
C.将溶解冷却的溶液转入容量瓶后就直接转入定容操作
D.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处
欲用98%的浓硫酸(g=1.84g·cm-3)配制成浓度为0.5mol·L-1的稀硫酸500ml。
(1)选用的仪器有:
①量筒 ②烧杯 ③玻璃棒 ④____________,⑤____________。
(2)下列各操作正确的顺序为____________________________。
A.用量筒量取浓H2SO4
B.反复颠倒摇匀
C.用胶头滴管加蒸馏水至刻度线
D.洗涤所用仪器2至3次,洗涤液也转入容量瓶中
E.稀释浓H2SO4
F.将溶液转入容量瓶
(3)简要回答下列问题:
①所需浓硫酸的体积为____________mL。
②浓硫酸稀释后在转入容量瓶前应____________,否则会使浓度偏____________。
③定容时必须使溶液液面与刻度线相切,若俯视会使浓度偏___________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com