
ĚâÄżÁбí(°üŔ¨´đ°¸şÍ˝âÎö)
 Ł¨2012?¸Ł˝¨Ł©Ł¨1Ł©µç¶ĆʱŁ¬¶ĆĽţÓëµçÔ´µÄ
Ł¨2012?¸Ł˝¨Ł©Ł¨1Ł©µç¶ĆʱŁ¬¶ĆĽţÓëµçÔ´µÄ(16·Ö)
(1)µç¶ĆʱŁ¬¶ĆĽţÓëµçÔ´µÄ Ľ«Á¬˝ÓˇŁ
(2)»ŻŃ§¶ĆµÄÔŔíĘÇŔűÓĂ»ŻŃ§·´Ó¦ÉúłÉ˝đĘôµĄÖĘłÁ»ýÔڶƼţ±íĂćĐγɶƲ㡣
˘Ů ČôÓĂÍŃνřĐĐ»ŻŃ§¶ĆÍŁ¬Ó¦ŃˇÓãߣ¨ĚŃő»ŻĽÁˇ±»ňˇ°»ąÔĽÁˇ±Ł©ÓëÖ®·´Ó¦ˇŁ
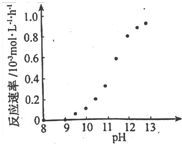
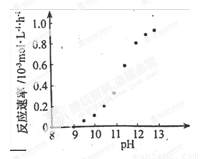
˘Ú Äł»ŻŃ§¶Ć͵ķ´Ó¦ËŮÂĘËć¶ĆŇşpH ±ä»ŻČçÓŇÍĽËůĘľˇŁ¸Ă¶ĆÍąýłĚÖĐŁ¬¶ĆŇşpH żŘÖĆÔÚ12.5×óÓҡŁľÝÍĽÖĐĐĹϢŁ¬¸řłöĘą·´Ó¦ÍŁÖąµÄ·˝·¨Łş 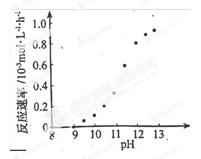
(3)Ëá˝ţ·¨ÖĆȡÁňËá͵ÄÁ÷łĚĘľŇâÍĽČçĎÂ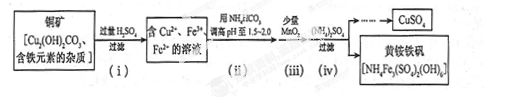
˘Ů ˛˝Ö裨iŁ©ÖĐCu2(OH) 2CO3·˘Éú·´Ó¦µÄ»ŻŃ§·˝łĚʽΪ ˇŁ
˘Ú ˛˝Ö裨iiŁ©ËůĽÓĘÔĽÁĆđµ÷˝ÚpH ×÷ÓõÄŔë×ÓĘÇ Ł¨ĚîŔë×Ó·űşĹŁ©ˇŁ
˘Ű ÔÚ˛˝Ö裨iiiŁ©·˘ÉúµÄ·´Ó¦ÖĐŁ¬1 mol MnO2תŇĆ2 mol µç×ÓŁ¬¸Ă·´Ó¦µÄŔë×Ó·˝łĚʽΪ ˇŁ
˘Ü ˛˝Ö裨ivŁ©łýČĄÔÓÖʵĻŻŃ§·˝łĚĘ˝żÉ±íʾΪ
3Fe3+ + NH4++2SO42-+6H2O= NH4Fe3 (SO4)2(OH)6Ł«6H +
ąýÂËşóĸҺµÄpH =" 2.0" , c (Fe3+) ="a" molˇ¤L-1Ł¬, c ( NH4+Ł©="b" molˇ¤L-1Ł¬, c ( SO42-Ł©=" d" molˇ¤L-1Ł¬¸Ă·´Ó¦µÄĆ˝şâłŁĘýK=Łß Ł¨ÓĂş¬a ˇ˘b ˇ˘d µÄ´úĘýĘ˝±íĘľŁ©ˇŁ
Ł¨1Ł©µç¶ĆĘÇŁ¬¶ĆĽţÓëµçÔ´µÄ Ľ«Á¬˝ÓˇŁ
Ł¨2Ł©»ŻŃ§¶ĆµÄÔŔíĘÇŔűÓĂ»ŻŃ§·´Ó¦ÉúłÉ˝đĘôµĄÖĘłÁµíÔڶƼţ±íĂćĐγɵĶƲ㡣
˘ŮČôÓĂÍŃνřĐĐ»ŻŃ§¶ĆÍŁ¬Ó¦Ńˇ
ÓĂ Ł¨ĚŃő»ŻĽÁˇ±»ňˇ°»ąÔĽÁˇ±Ł©ÓëÖ®·´Ó¦ˇŁ
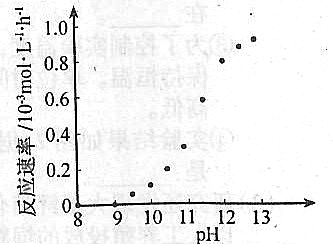
˘ÚÄł»ŻŃ§¶Ć͵ķ´Ó¦ËŮÂĘËć¶ĆŇşpH±ä»ŻČçÓŇÍĽËůĘľˇŁ¸Ă¶ĆÍąýłĚÖĐŁ¬¶ĆŇşpHżŘÖĆÔÚ12.5×óÓҡŁľÝÍĽÖĐĐĹϢŁ¬¸řłöĘą·´Ó¦ÍŁÖąµÄ·˝·¨Łş
Ł¨3Ł©Ëá˝ţ·¨ÖĆȡÁňËá͵ÄÁ÷łĚĘľŇâÍĽČçĎÂŁş
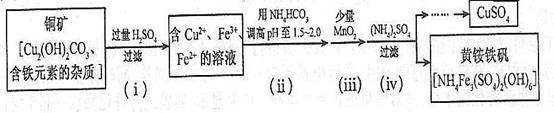
˘Ů˛˝Ö裨iŁ©ÖĐCu2(OH)2CO3·˘Éú·´Ó¦µÄ»ŻŃ§·˝łĚʽΪ ˇŁ
˘Ú˛˝Ö裨iiŁ©ËůĽÓĘÔĽÁĆđµ÷˝ÚpH×÷ÓõÄŔë×ÓĘÇ (ĚîŔë×Ó·űşĹ)ˇŁ
˘ŰÔÚ˛˝Ö裨iiiŁ©·˘ÉúµÄ·´Ó¦ÖĐŁ¬1molMnO2תŇĆ2¸ömolµç×ÓŁ¬¸Ă·´Ó¦µÄŔë×Ó·˝łĚʽΪ ˇŁ
˘Ü˛˝Ö裨ivŁ©łýČĄÔÓÖʵĻŻŃ§·˝łĚĘ˝żÉ±íʾΪ
![]()
ąýÂËşóĸҺµÄpH=2.0Ł¬cŁ¨![]() Ł©=a molˇ¤LˇŞ1Ł¬cŁ¨
Ł©=a molˇ¤LˇŞ1Ł¬cŁ¨![]() Ł©=b molˇ¤LˇŞ1Ł¬cŁ¨
Ł©=b molˇ¤LˇŞ1Ł¬cŁ¨![]() Ł©=d molˇ¤LˇŞ1Ł¬¸Ă·´Ó¦µÄĆ˝şâłŁĘýK= Ł¨ÓĂş¬aˇ˘bˇ˘dµÄ´úĘýĘ˝±íĘľŁ©ˇŁ
Ł©=d molˇ¤LˇŞ1Ł¬¸Ă·´Ó¦µÄĆ˝şâłŁĘýK= Ł¨ÓĂş¬aˇ˘bˇ˘dµÄ´úĘýĘ˝±íĘľŁ©ˇŁ
(16·Ö)
(1)µç¶ĆʱŁ¬¶ĆĽţÓëµçÔ´µÄ Ľ«Á¬˝ÓˇŁ
(2)»ŻŃ§¶ĆµÄÔŔíĘÇŔűÓĂ»ŻŃ§·´Ó¦ÉúłÉ˝đĘôµĄÖĘłÁ»ýÔڶƼţ±íĂćĐγɶƲ㡣
˘Ů ČôÓĂÍŃνřĐĐ»ŻŃ§¶ĆÍŁ¬Ó¦ŃˇÓãߣ¨ĚŃő»ŻĽÁˇ±»ňˇ°»ąÔĽÁˇ±Ł©ÓëÖ®·´Ó¦ˇŁ
˘Ú Äł»ŻŃ§¶Ć͵ķ´Ó¦ËŮÂĘËć¶ĆŇşpH ±ä»ŻČçÓŇÍĽËůĘľˇŁ¸Ă¶ĆÍąýłĚÖĐŁ¬¶ĆŇşpH żŘÖĆÔÚ12.5×óÓҡŁľÝÍĽÖĐĐĹϢŁ¬¸řłöĘą·´Ó¦ÍŁÖąµÄ·˝·¨Łş
(3)Ëá˝ţ·¨ÖĆȡÁňËá͵ÄÁ÷łĚĘľŇâÍĽČçĎÂ
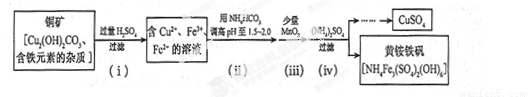
˘Ů ˛˝Ö裨iŁ©ÖĐCu2(OH) 2CO3 ·˘Éú·´Ó¦µÄ»ŻŃ§·˝łĚʽΪ ˇŁ
˘Ú ˛˝Ö裨iiŁ©ËůĽÓĘÔĽÁĆđµ÷˝ÚpH ×÷ÓõÄŔë×ÓĘÇ Ł¨ĚîŔë×Ó·űşĹŁ©ˇŁ
˘Ű ÔÚ˛˝Ö裨iiiŁ©·˘ÉúµÄ·´Ó¦ÖĐŁ¬1 mol MnO2תŇĆ2 mol µç×ÓŁ¬¸Ă·´Ó¦µÄŔë×Ó·˝łĚʽΪ ˇŁ
˘Ü ˛˝Ö裨ivŁ©łýČĄÔÓÖʵĻŻŃ§·˝łĚĘ˝żÉ±íʾΪ
3Fe3+ + NH4++2SO42-+6H2O= NH4Fe3 (SO4)2(OH)6Ł«6H +
ąýÂËşóĸҺµÄpH = 2.0 , c (Fe3+) =a molˇ¤L-1Ł¬, c ( NH4+Ł©=b molˇ¤L-1Ł¬, c ( SO42-Ł©= d molˇ¤L-1Ł¬¸Ă·´Ó¦µÄĆ˝şâłŁĘýK=Łß Ł¨ÓĂş¬a ˇ˘b ˇ˘d µÄ´úĘýĘ˝±íĘľŁ©ˇŁ

ąúĽĘѧУÓĹѡ - Á·Ď°˛áÁбí - ĘÔĚâÁбí
şţ±±Ęˇ»ĄÁŞÍřÎĄ·¨şÍ˛»ÁĽĐĹϢľŮ±¨Ć˝Ě¨ | ÍřÉĎÓĐş¦ĐĹϢľŮ±¨×¨Çř | µçĐĹթƾٱ¨×¨Çř | ÉćŔúĘ·ĐéÎŢÖ÷ŇĺÓĐş¦ĐĹϢľŮ±¨×¨Çř | ÉćĆóÇÖȨľŮ±¨×¨Çř
ÎĄ·¨şÍ˛»ÁĽĐĹϢľŮ±¨µç»°Łş027-86699610 ľŮ±¨ÓĘĎ䣺58377363@163.com