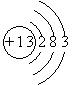
有①~⑩十种元素,原子序数依次增大,⑨、⑩为第四周期过渡元素,其余均为短周期元素.

(1)若②、⑦、⑧三种元素在周期表中相对位置如下:
由②形成的化合物种类最多,则②、⑦、⑧三种元素最高价氧化物的水化物酸性由强到弱的顺序是
HClO4>H2SO4>H2CO3
HClO4>H2SO4>H2CO3
(用化学式表示).
(2)甲、乙、丙、丁、戊均为上述短周期元素中的某些单质或由其中两种元素组成的化合物,且甲、戊为无色气体,反应a为置换反应,反应b为化合反应.见右图示转化关系推测:戊可能为
CO、SO2、NO
CO、SO2、NO
(列举一例).
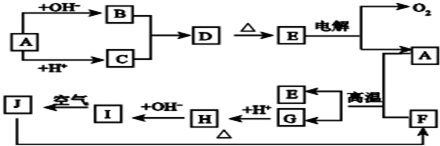
(3)若图1中A、B、C、D、E分别是上述10种元素中的某些单质或其中两种元素组成的化合物.已知:A是常见金属,D、E分别为无色和黄绿色气体,反应c是用A作电极,在B的水溶液中进行的电解反应,属于置换反应类型.它们的转化关系如图2示.则反应d中阴极的电极反应式为
Cu2++2e-═Cu
Cu2++2e-═Cu
.
若反应c是在高温下进行的,且为工业上有重要应用价值的放热反应,物质C是一种两性化合物,则反应c的化学方程式
.

 置换反应的通式可表示为(转化中涉及的均为中学化学的常见物质):
置换反应的通式可表示为(转化中涉及的均为中学化学的常见物质):