
题目列表(包括答案和解析)
A.该反应可能是化合反应,也可能是氧化还原反应
B.该反应一定是复分解反应,且属于非氧化还原反应
C.该反应可能是CaCl2+Na2CO3===CaCO3↓+2NaCl
D.该反应可能是Ca(OH)2+K2CO3===CaCO3↓+2KOH
某反应的离子方程式为Ca2++CO![]()
![]() CaCO3↓,对该反应的下列说法不正确的是( )
CaCO3↓,对该反应的下列说法不正确的是( )
A.该反应可能是化合反应,也可能是氧化还原反应
B.该反应一定是复分解反应,且属于非氧化还原反应
C.该反应可能是CaCl2+Na2CO3![]() CaCO3↓+2NaCl
CaCO3↓+2NaCl
D.该反应可能是Ca(OH)2+K2CO3![]() CaCO3↓+2KOH
CaCO3↓+2KOH
| ||
| ||
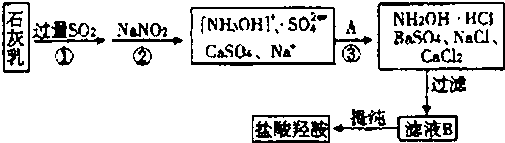
完成下列问题:?
(1)写出下列物质的化学式:X ,G ,?D ?。?
(2)写出G与C反应生成D的化学方程式:?
。?
(3)写出X+E![]() A的离子方程式: 。?
A的离子方程式: 。?
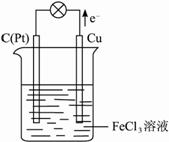
Ⅱ.某反应的离子方程式为2Fe3++Cu=2Fe2++Cu2+,试设计一个原电池实现该反应。?
(1)该原电池的电极反应式为:?
正极 ;?
负极 。?
(2)该原电池正极材料为 ,负极材料为 ,电解质溶液是 。?
(3)画出该原电池的示意图,并标出电子流动的方向。?

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com