
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
| —ŒÀ·Ãª˝£®mL£© | 8 | 15 | 20 | 50 | x | 120 | 150 |
| …˙≥…CO2ê˝£®mL£© | 0 | 112 | 224 | 896 | 2240 | 2240 | 2240 |
°∞«‚ƒÐ°±Ω´ «Œ¥¿¥◊ӿ̜εƒ–¬ƒÐ‘¥°£
¢Ò. µ—È≤‚µ√£¨1g«‚∆¯»º…’…˙≥…“∫èÀÆ ±∑≈≥ˆ142.9kJ»»¡ø£¨‘Ú«‚∆¯»º…’µƒ»»ªØ—ß∑Ω≥Ã ΩŒ™_______°££®ÃÓ–Ú∫≈£©
A.2H2£®g£©+O2£®g£© ![]() 2H2O£®l£© °˜H= £≠142.9kJ°§mol°™1
2H2O£®l£© °˜H= £≠142.9kJ°§mol°™1
B.H2£®g£©+1/2 O2£®g£© ![]() H2O£®l£© °˜H= £≠285.8kJ°§mol°™1
H2O£®l£© °˜H= £≠285.8kJ°§mol°™1
C.2H2+O2![]() 2H2O£®l£© °˜H= £≠571.6kJ°§mol°™1
2H2O£®l£© °˜H= £≠571.6kJ°§mol°™1
D.H2£®g£©+1/2O2£®g£© ![]() H2O£®g£© °˜H= £≠285.8kJ°§mol°™1
H2O£®g£© °˜H= £≠285.8kJ°§mol°™1
¢Ú.ƒ≥ªØ—ߺ“∏˘æð°∞‘≠◊”æ≠º√°±µƒÀºœÎ£¨…˺∆¡À»Áœ¬÷∆±∏H2µƒ∑¥”¶≤Ω÷Ë
¢ŸCaBr2+H2O![]() CaO+2HBr ¢⁄2HBr+Hg
CaO+2HBr ¢⁄2HBr+Hg![]() HgBr2+H2
HgBr2+H2
¢€HgBr2+_____![]() ______________ ¢Ð2HgO
______________ ¢Ð2HgO 2Hg+O2°¸
2Hg+O2°¸
«Îƒ„∏˘æð°∞‘≠◊”æ≠º√°±µƒÀºœÎÕÍ≥……œ ˆ≤Ω÷Ë¢€µƒªØ—ß∑Ω≥Ã Ω£∫____________°£
∏˘æð°∞¬Ã…´ªØ—ß°±µƒÀºœÎ∆¿π¿∏√∑Ω∑®÷∆H2µƒ÷˜“™»±µ„£∫______________°£
¢Û.¿˚”√∫ÀƒÐ∞—ÀÆ∑÷Ω‚÷∆«‚∆¯£¨ «ƒø«∞’˝‘⁄—–æøµƒøŒÃ‚°£œ¬Õº «∆‰÷–µƒ“ª÷÷¡˜≥ã¨∆‰÷–”√¡Àπ˝¡øµƒµ‚°££®Ã· æ£∫∑¥”¶¢⁄µƒ≤˙ŒÔ «O2°¢SO2∫ÕH2O£©

ÕÍ≥…œ¬¡–∑¥”¶µƒªØ—ß∑Ω≥Ã Ω£∫
∑¥”¶¢Ÿ__________________________£ª∑¥”¶¢⁄__________________________°£
¥À∑®÷∆»°«‚∆¯µƒ◊Ó¥Û”≈µ„ «_______________________________________________°£
¢Ù.«‚∆¯Õ®≥£”√…˙≤˙ÀÆ√∫∆¯µƒ∑Ω∑®÷∆µ√°£∆‰÷–CO£®g£©+ H2O£®g£© CO2£®g£©+ H2£®g£©; °˜H<0°£
‘⁄850°Ê ±£¨K=1°£
£®1£©»Ù…˝∏þŒ¬∂»µΩ950°Ê ±£¨¥ÔµΩ∆Ω∫‚ ±K______1£®ÃÓ°∞¥Û”⁄°±°¢°∞–°”⁄°±ªÚ°∞µ»”⁄°±£©
£®2£©850°Ê ±£¨»ÙœÚ“ª»ðª˝ø…±‰µƒ√б’»ð∆˜÷–Õ¨ ±≥‰»Î 1.0 mol CO°¢3.0molH2O°¢1.0mol CO2 ∫Õ x mol H2£¨‘Ú£∫
¢Ÿµ±x=5.0 ±£¨…œ ˆ∆Ω∫‚œÚ___________£®ÃÓ’˝∑¥”¶ªÚƒÊ∑¥”¶£©∑ΩœÚΩ¯––°£
¢⁄»Ù“™ π…œ ˆ∑¥”¶ø™ º ±œÚ’˝∑¥”¶∑ΩœÚΩ¯––£¨‘Úx”¶¬˙◊„µƒÃıº˛ «__________°£
£®3£©‘⁄850°Ê ±£¨»Ù…Ëx£Ω5.0mol∫Õx£Ω6.0mol£¨∆‰À¸ŒÔ÷ µƒÕ∂¡œ≤ª±‰£¨µ±…œ ˆ∑¥”¶¥ÔµΩ∆Ω∫‚∫Û£¨≤‚µ√H2µƒÃª˝∑÷ ˝∑÷±Œ™a£•°¢b£•£¨‘Úa_______ b£®ÃÓ°∞¥Û”⁄°±°¢°∞–°”⁄°±ªÚ°∞µ»”⁄°±£©°£
¢ı.«‚∆¯ªπ‘≠—ıªØÕ≠À˘µ√µƒ∫Ï…´πÃÃÂø…ƒÐ «Õ≠”ΗıªØ—«Õ≠µƒªÏ∫œŒÔ£¨“—÷™Cu2O‘⁄À·–‘»Ð“∫÷–ø…∑¢…˙◊‘…Ì—ıªØªπ‘≠∑¥”¶£¨…˙≥…Cu2+∫Õµ•÷ Õ≠°£
£®1£©œ÷”–8øÀ—ıªØÕ≠±ª«‚∆¯ªπ‘≠∫Û£¨µ√µΩ∫Ï…´πÃÃÂ6.8øÀ£¨∆‰÷–∫¨µ•÷ Õ≠”ΗıªØ—«Õ≠µƒŒÔ÷ µƒ¡ø÷Ʊ» « £ª
£®2£©»ÙΩ´6.8øÀ…œ ˆªÏ∫œŒÔ”Î◊„¡øµƒœ°¡ÚÀ·≥‰∑÷∑¥”¶∫Ûπ˝¬À£¨ø…µ√µΩπÃàg£ª
£®3£©»ÙΩ´6.8øÀ…œ ˆªÏ∫œŒÔ”Γª∂®¡øµƒ≈®œıÀ·≥‰∑÷∑¥”¶£¨
¢Ÿ…˙≥…±Í◊º◊¥øˆœ¬1.568…˝µƒ∆¯Ã£®≤ªøº¬«NO2µƒ»ÐΩ‚£¨“≤≤ªøº¬«NO2”ÎN2O4µƒ◊™ªØ£©£¨‘Ú∏√∆¯Ãµƒ≥…∑÷ « £¨∆‰ŒÔ÷ µƒ¡ø÷Ʊ» « £ª
¢⁄∞—µ√µΩµƒ»Ð“∫–°–ƒ’Ù∑¢≈®Àı£¨∞—Œˆ≥ˆµƒæßÃÂπ˝¬À£¨µ√æßÃÂ23.68g°£æ≠∑÷Œˆ£¨‘≠»Ð“∫÷–µƒCu2+”–20%≤–¡Ù‘⁄ƒ∏“∫÷–°£«ÛÀ˘µ√æßõƒªØ—ß Ω
°∞«‚ƒÐ°±Ω´ «Œ¥¿¥◊ӿ̜εƒ–¬ƒÐ‘¥£Æ
¢Ò£Æ µ—È≤‚µ√£¨1 g«‚∆¯»º…’…˙≥…“∫èÀÆ ±∑≈≥ˆ142.9 kJ»»¡ø£¨‘Ú«‚∆¯»º…’µƒ»»ªØ—ß∑Ω≥Ã ΩŒ™________£Æ(ÃÓ–Ú∫≈)
A£Æ
2H2(g)£´O2(g)B£ÆH2(g)£´1/2O2(g)![]() H2O(l)°°¶§H£Ω£≠285.8 kJ°§mol£≠1
H2O(l)°°¶§H£Ω£≠285.8 kJ°§mol£≠1
C£Æ2H2£´O2![]() 2H2O(l)°°¶§H£Ω£≠571.6 kJ°§mol£≠1
2H2O(l)°°¶§H£Ω£≠571.6 kJ°§mol£≠1
D£ÆH2(g)£´1/2O2(g)![]() H2O(g)°°¶§H£Ω£≠285.8 kJ°§mol£≠1
H2O(g)°°¶§H£Ω£≠285.8 kJ°§mol£≠1
¢Ú
£Æƒ≥ªØ—ߺ“∏˘æð°∞‘≠◊”æ≠º√°±µƒÀºœÎ£¨…˺∆¡À»Áœ¬÷∆±∏H2µƒ∑¥”¶≤Ω÷Ë¢ŸCaBr2£´H2O CaO£´2HBr
CaO£´2HBr
¢⁄2HBr£´Hg HgBr2£´H2
HgBr2£´H2
¢€HgBr2£´________ ________
________
¢Ð2HgO 2Hg£´O2°¸
2Hg£´O2°¸
«Îƒ„∏˘æð°∞‘≠◊”æ≠º√°±µƒÀºœÎÕÍ≥……œ ˆ≤Ω÷Ë¢€µƒªØ—ß∑Ω≥Ã Ω£∫________£Æ
∏˘æð°∞
¬Ã…´ªØ—ß°±µƒÀºœÎ∆¿π¿∏√∑Ω∑®÷∆H2µƒ÷˜“™»±µ„£∫________£Æ¢Û
£Æ¿˚”√∫ÀƒÐ∞—ÀÆ∑÷Ω‚÷∆«‚∆¯£¨ «ƒø«∞’˝‘⁄—–æøµƒøŒÃ‚£Æœ¬Õº «∆‰÷–µƒ“ª÷÷¡˜≥ã¨∆‰÷–”√¡Àπ˝¡øµƒµ‚£Æ(÷ æ£∫∑¥”¶¢⁄µƒ≤˙ŒÔ «O2°¢SO2∫ÕH2O)
ÕÍ≥…œ¬¡–
∑¥”¶µƒªØ—ß∑Ω≥Ã Ω£∫∑¥”¶¢Ÿ________£ª∑¥”¶¢⁄________£Æ
¥À∑®÷∆»°
«‚∆¯µƒ◊Ó¥Û”≈µ„ «________£Æ¢Ù
£Æ«‚∆¯Õ®≥£”√…˙≤˙ÀÆ√∫∆¯µƒ∑Ω∑®÷∆µ√£Æ∆‰÷–CO(g)£´H2O(g)(1)»Ù…˝∏þŒ¬∂»µΩ950°Ê ±£¨¥ÔµΩ∆Ω∫‚ ±K________1(ÃÓ°∞¥Û”⁄°±°¢°∞–°”⁄°±ªÚ°∞µ»”⁄°±)
(2)850°Ê ±£¨»ÙœÚ“ª»ðª˝ø…±‰µƒ√б’»ð∆˜÷–Õ¨ ±≥‰»Î1.0 mol°°CO°¢3.0 mol°°H2O°¢1.0 mol°°CO2∫Õx mol°°H2£¨‘Ú£∫
¢Ÿµ±x£Ω5.0 ±£¨…œ ˆ∆Ω∫‚œÚ________(ÃÓ’˝∑¥”¶ªÚƒÊ∑¥”¶)∑ΩœÚΩ¯––£Æ
¢⁄»Ù“™ π…œ ˆ∑¥”¶ø™ º ±œÚ’˝∑¥”¶∑ΩœÚΩ¯––£¨‘Úx”¶¬˙◊„µƒÃıº˛ «________£Æ
(3)‘⁄850°Ê ±£¨»Ù…Ëx£Ω5.0 mol∫Õx£Ω6.0 mol£¨∆‰À¸ŒÔ÷ µƒÕ∂¡œ≤ª±‰£¨µ±…œ ˆ∑¥”¶¥ÔµΩ∆Ω∫‚∫Û£¨≤‚µ√H2µƒÃª˝∑÷ ˝∑÷±Œ™a£•°¢b£•£¨‘Úa________b(ÃÓ°∞¥Û”⁄°±°¢°∞–°”⁄°±ªÚ°∞µ»”⁄°±)£Æ
¢ı
£Æ«‚∆¯ªπ‘≠—ıªØÕ≠À˘µ√µƒ∫Ï…´πÃÃÂø…ƒÐ «Õ≠”ΗıªØ—«Õ≠µƒªÏ∫œŒÔ£¨“—÷™Cu2O‘⁄À·–‘»Ð“∫÷–ø…∑¢…˙◊‘…Ì—ıªØªπ‘≠∑¥”¶£¨…˙≥…Cu2+∫Õµ•÷ Õ≠£Æ(1)œ÷”–8øÀ—ıªØÕ≠±ª«‚∆¯ªπ‘≠∫Û£¨µ√µΩ∫Ï…´πÃÃÂ6.8øÀ£¨∆‰÷–∫¨µ•÷ Õ≠”ΗıªØ—«Õ≠µƒŒÔ÷ µƒ¡ø÷Ʊ» «________£ª
(2)»ÙΩ´6.8øÀ…œ ˆªÏ∫œŒÔ”Î◊„¡øµƒœ°¡ÚÀ·≥‰∑÷∑¥”¶∫Ûπ˝¬À£¨ø…µ√µΩπÃÃÂ________g£ª
(3)»ÙΩ´6.8øÀ…œ ˆªÏ∫œŒÔ”Γª∂®¡øµƒ≈®œıÀ·≥‰∑÷∑¥”¶£¨
¢Ÿ…˙≥…±Í◊º◊¥øˆœ¬1.568…˝µƒ∆¯ÃÂ(≤ªøº¬«NO2µƒ»ÐΩ‚£¨“≤≤ªøº¬«NO2”ÎN2O4µƒ◊™ªØ)£¨‘Ú∏√∆¯Ãµƒ≥…∑÷ «________£¨∆‰ŒÔ÷ µƒ¡ø÷Ʊ» «________£ª
¢⁄∞—µ√µΩµƒ»Ð“∫–°–ƒ’Ù∑¢≈®Àı£¨∞—Œˆ≥ˆµƒæßÃÂπ˝¬À£¨µ√æßÃÂ23.68 g£Ææ≠∑÷Œˆ£¨‘≠»Ð“∫÷–µƒCu2+”–20£•≤–¡Ù‘⁄ƒ∏“∫÷–£Æ«ÛÀ˘µ√æßõƒªØ—ß Ω
°∞«‚ƒÐ°±Ω´ «Œ¥¿¥◊ӿ̜εƒ–¬ƒÐ‘¥°£
¢Ò. µ—È≤‚µ√£¨1g«‚∆¯»º…’…˙≥…“∫èÀÆ ±∑≈≥ˆ142.9kJ»»¡ø£¨‘Ú«‚∆¯»º…’µƒ»»ªØ—ß∑Ω≥Ã ΩŒ™_______°££®ÃÓ–Ú∫≈£©
A.2H2£®g£©+O2£®g£©  2H2O£®l£©
°˜H= £≠142.9kJ°§mol°™1
2H2O£®l£©
°˜H= £≠142.9kJ°§mol°™1
B.H2£®g£©+1/2 O2£®g£©  H2O£®l£©
°˜H= £≠285.8kJ°§mol°™1
H2O£®l£©
°˜H= £≠285.8kJ°§mol°™1
C.2H2+O2 2H2O£®l£©
°˜H= £≠571.6kJ°§mol°™1
2H2O£®l£©
°˜H= £≠571.6kJ°§mol°™1
D.H2£®g£©+1/2
O2£®g£©  H2O£®g£© °˜H= £≠285.8kJ°§mol°™1
H2O£®g£© °˜H= £≠285.8kJ°§mol°™1
¢Ú.ƒ≥ªØ—ߺ“∏˘æð°∞‘≠◊”æ≠º√°±µƒÀºœÎ£¨…˺∆¡À»Áœ¬÷∆±∏H2µƒ∑¥”¶≤Ω÷Ë
¢ŸCaBr2+H2O CaO+2HBr ¢⁄2HBr+Hg
CaO+2HBr ¢⁄2HBr+Hg HgBr2+H2
HgBr2+H2
¢€HgBr2+_____ ______________
¢Ð2HgO
______________
¢Ð2HgO 2Hg+O2°¸
2Hg+O2°¸
«Îƒ„∏˘æð°∞‘≠◊”æ≠º√°±µƒÀºœÎÕÍ≥……œ ˆ≤Ω÷Ë¢€µƒªØ—ß∑Ω≥Ã Ω£∫____________°£
∏˘æð°∞¬Ã…´ªØ—ß°±µƒÀºœÎ∆¿π¿∏√∑Ω∑®÷∆H2µƒ÷˜“™»±µ„£∫______________°£
¢Û.¿˚”√∫ÀƒÐ∞—ÀÆ∑÷Ω‚÷∆«‚∆¯£¨ «ƒø«∞’˝‘⁄—–æøµƒøŒÃ‚°£œ¬Õº «∆‰÷–µƒ“ª÷÷¡˜≥ã¨∆‰÷–”√¡Àπ˝¡øµƒµ‚°££®Ã· æ£∫∑¥”¶¢⁄µƒ≤˙ŒÔ «O2°¢SO2∫ÕH2O£©

ÕÍ≥…œ¬¡–∑¥”¶µƒªØ—ß∑Ω≥Ã Ω£∫
∑¥”¶¢Ÿ__________________________£ª∑¥”¶¢⁄__________________________°£
¥À∑®÷∆»°«‚∆¯µƒ◊Ó¥Û”≈µ„ «_______________________________________________°£
¢Ù.«‚∆¯Õ®≥£”√…˙≤˙ÀÆ√∫∆¯µƒ∑Ω∑®÷∆µ√°£∆‰÷–CO£®g£©+ H2O£®g£© 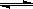 CO2£®g£©+ H2£®g£©; °˜H<0°£
CO2£®g£©+ H2£®g£©; °˜H<0°£
‘⁄850°Ê ±£¨K=1°£
£®1£©»Ù…˝∏þŒ¬∂»µΩ950°Ê ±£¨¥ÔµΩ∆Ω∫‚ ±K______1£®ÃÓ°∞¥Û”⁄°±°¢°∞–°”⁄°±ªÚ°∞µ»”⁄°±£©
£®2£©850°Ê ±£¨»ÙœÚ“ª»ðª˝ø…±‰µƒ√б’»ð∆˜÷–Õ¨ ±≥‰»Î 1.0 mol CO°¢3.0molH2O°¢1.0mol CO2 ∫Õ x mol H2£¨‘Ú£∫
¢Ÿµ±x=5.0 ±£¨…œ ˆ∆Ω∫‚œÚ___________£®ÃÓ’˝∑¥”¶ªÚƒÊ∑¥”¶£©∑ΩœÚΩ¯––°£
¢⁄»Ù“™ π…œ ˆ∑¥”¶ø™ º ±œÚ’˝∑¥”¶∑ΩœÚΩ¯––£¨‘Úx”¶¬˙◊„µƒÃıº˛ «__________°£
£®3£©‘⁄850°Ê ±£¨»Ù…Ëx£Ω5.0 mol∫Õx£Ω6.0mol£¨∆‰À¸ŒÔ÷ µƒÕ∂¡œ≤ª±‰£¨µ±…œ ˆ∑¥”¶¥ÔµΩ∆Ω∫‚∫Û£¨≤‚µ√H2µƒÃª˝∑÷ ˝∑÷±Œ™a£•°¢b£•£¨‘Úa _______ b£®ÃÓ°∞¥Û”⁄°±°¢°∞–°”⁄°±ªÚ°∞µ»”⁄°±£©°£
¢ı.«‚∆¯ªπ‘≠—ıªØÕ≠À˘µ√µƒ∫Ï…´πÃÃÂø…ƒÐ «Õ≠”ΗıªØ—«Õ≠µƒªÏ∫œŒÔ£¨“—÷™Cu2O‘⁄À·–‘»Ð“∫÷–ø…∑¢…˙◊‘…Ì—ıªØªπ‘≠∑¥”¶£¨…˙≥…Cu2+∫Õµ•÷ Õ≠°£
£®1£©œ÷”–8øÀ—ıªØÕ≠±ª«‚∆¯ªπ‘≠∫Û£¨µ√µΩ∫Ï…´πÃÃÂ6.8øÀ£¨∆‰÷–∫¨µ•÷ Õ≠”ΗıªØ—«Õ≠µƒŒÔ÷ µƒ¡ø÷Ʊ» « £ª
£®2£©»ÙΩ´6.8øÀ…œ ˆªÏ∫œŒÔ”Î◊„¡øµƒœ°¡ÚÀ·≥‰∑÷∑¥”¶∫Ûπ˝¬À£¨ø…µ√µΩπÃàg£ª
£®3£©»ÙΩ´6.8øÀ…œ ˆªÏ∫œŒÔ”Γª∂®¡øµƒ≈®œıÀ·≥‰∑÷∑¥”¶£¨
¢Ÿ…˙≥…±Í◊º◊¥øˆœ¬1.568…˝µƒ∆¯Ã£®≤ªøº¬«NO2µƒ»ÐΩ‚£¨“≤≤ªøº¬«NO2”ÎN2O4µƒ◊™ªØ£©£¨‘Ú∏√∆¯Ãµƒ≥…∑÷ « £¨∆‰ŒÔ÷ µƒ¡ø÷Ʊ» « £ª
¢⁄∞—µ√µΩµƒ»Ð“∫–°–ƒ’Ù∑¢≈®Àı£¨∞—Œˆ≥ˆµƒæßÃÂπ˝¬À£¨µ√æßÃÂ23.68g°£æ≠∑÷Œˆ£¨‘≠»Ð“∫÷–µƒCu2+”–20%≤–¡Ù‘⁄ƒ∏“∫÷–°£«ÛÀ˘µ√æßõƒªØ—ß Ω
°∞«‚ƒÐ°±Ω´ «Œ¥¿¥◊ӿ̜εƒ–¬ƒÐ‘¥°£
¢Ò. µ—È≤‚µ√£¨1g«‚∆¯»º…’…˙≥…“∫èÀÆ ±∑≈≥ˆ142.9kJ»»¡ø£¨‘Ú«‚∆¯»º…’µƒ»»ªØ—ß∑Ω≥Ã ΩŒ™_______°££®ÃÓ–Ú∫≈£©
A£Æ2H2£®g£©+O2£®g£©  2H2O£®l£©°˜H= £≠142.9kJ°§mol°™1 2H2O£®l£©°˜H= £≠142.9kJ°§mol°™1 |
B£ÆH2£®g£©+1/2 O2£®g£©  H2O£®l£©°˜H= £≠285.8kJ°§mol°™1 H2O£®l£©°˜H= £≠285.8kJ°§mol°™1 |
C£Æ2H2+O2 2H2O£®l£©°˜H= £≠571.6kJ°§mol°™1 2H2O£®l£©°˜H= £≠571.6kJ°§mol°™1 |
D£ÆH2£®g£©+1/2 O2£®g£©  H2O£®g£© °˜H= £≠285.8kJ°§mol°™1 H2O£®g£© °˜H= £≠285.8kJ°§mol°™1 |
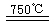 CaO+2HBr ¢⁄2HBr+Hg
CaO+2HBr ¢⁄2HBr+Hg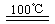 HgBr2+H2
HgBr2+H2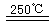 ______________ ¢Ð2HgO
______________ ¢Ð2HgO 2Hg+O2°¸
2Hg+O2°¸
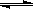 CO2£®g£©+ H2£®g£©; °˜H<0°£
CO2£®g£©+ H2£®g£©; °˜H<0°£π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com