
题目列表(包括答案和解析)
下列反应中不可能设计成原电池的是( )
A.NaOH+HCl===NaCl+H2O B.2Fe3++Fe===3Fe2+
C.Zn+2HCl===ZnCl2+H2↑ D.4Al+3O2+6H2O===4Al(OH)3↓
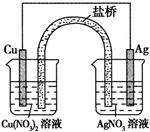 (1)实验证明能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是
(1)实验证明能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是
|
|
|
| O | - 3 |
| ||
| ||
下列说法中正确的是( )
A.凡是放热反应都是自发的,吸热反应都是非自发的
B.在反应A(g)+3B(g)=2C(g)+2D(g)的速率测定实验中,分别测得反应速率如下:v(A)= 0.15mol·L-1·s-1,
v (C)=0.3 mol·L-1·s-1,则用C来表示反应进行的速率更快。
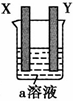
C.如图所示,在一U型管中装入含有紫色石蕊试液的Na2SO4溶液,通直流电,一段时间后U型管内会形成一个倒立的三色“彩虹”,从左到右颜色的次序是:红、紫、蓝

D.反应HCl(aq) + NaOH(aq) = NaCl (aq) + H2O(l) △H < 0, 在理论上能用于设计原电池。
下列说法中正确的是
A.凡是放热反应都是自发的,吸热反应都是非自发的
B.在反应A(g)+3B(g)=2C(g)+2D(g) 的速率测定实验中,分别 测得反应速率如下:v(A)= 0.15mol·L—1·s—1 ,v(C)= 0.3 mol·L—1·s—1 ,则用C来表示反应进行的速率更快。
C.如图所示,在一U型管中装入含有紫色石蕊试液的Na2SO4溶液,通直流电,一段时间后U型管内会形成一个倒立的三色“彩虹”,从左到右颜色的次序是.红、紫、蓝

D.反应HCl ( aq ) + NaOH ( aq ) = NaCl ( aq ) + H2O ( l ) △H < 0,在理论上能用于设计原电池
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com