
جâؤ؟ءذ±ي(°üہ¨´ً°¸؛ح½âخِ)
 2HI£¨g£©
2HI£¨g£©
 2HI£¨g£©
2HI£¨g£©،°اâؤـ،±½«تاخ´ہ´×îہيدëµؤذآؤـش´،£
¢ٌ.تµرé²âµأ£¬1gاâئّب¼ةصةْ³ةز؛ج¬ث®ت±·إ³ِ142.9kJببء؟£¬شٍاâئّب¼ةصµؤبب»¯ر§·½³جت½خھ_______،££¨جîذٍ؛إ£©
A£®2H2£¨g£©+O2£¨g£©  2H2O£¨l£©،÷H= £142.9kJ،¤mol،ھ1 2H2O£¨l£©،÷H= £142.9kJ،¤mol،ھ1 |
B£®H2£¨g£©+1/2 O2£¨g£©  H2O£¨l£©،÷H= £285.8kJ،¤mol،ھ1 H2O£¨l£©،÷H= £285.8kJ،¤mol،ھ1 |
C£®2H2+O2 2H2O£¨l£©،÷H= £571.6kJ،¤mol،ھ1 2H2O£¨l£©،÷H= £571.6kJ،¤mol،ھ1 |
D£®H2£¨g£©+1/2 O2£¨g£©  H2O£¨g£© ،÷H= £285.8kJ،¤mol،ھ1 H2O£¨g£© ،÷H= £285.8kJ،¤mol،ھ1 |
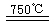 CaO+2HBr ¢ع2HBr+Hg
CaO+2HBr ¢ع2HBr+Hg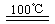 HgBr2+H2
HgBr2+H2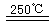 ______________ ¢ـ2HgO
______________ ¢ـ2HgO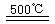 2Hg+O2،ü
2Hg+O2،ü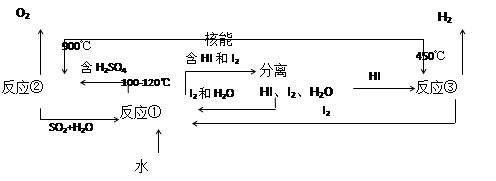
 CO2£¨g£©+ H2£¨g£©; ،÷H<0،£
CO2£¨g£©+ H2£¨g£©; ،÷H<0،£A£®2H2£¨g£©+O2£¨g£©  2H2O£¨l£©،÷H= £142.9kJ،¤mol،ھ1 2H2O£¨l£©،÷H= £142.9kJ،¤mol،ھ1 |
B£®H2£¨g£©+1/2 O2£¨g£©  H2O£¨l£©،÷H= £285.8kJ،¤mol،ھ1 H2O£¨l£©،÷H= £285.8kJ،¤mol،ھ1 |
C£®2H2+O2 2H2O£¨l£©،÷H= £571.6kJ،¤mol،ھ1 2H2O£¨l£©،÷H= £571.6kJ،¤mol،ھ1 |
D£®H2£¨g£©+1/2 O2£¨g£©  H2O£¨g£© ،÷H= £285.8kJ،¤mol،ھ1 H2O£¨g£© ،÷H= £285.8kJ،¤mol،ھ1 |
 CaO+2HBr ¢ع2HBr+Hg
CaO+2HBr ¢ع2HBr+Hg HgBr2+H2
HgBr2+H2 ______________ ¢ـ2HgO
______________ ¢ـ2HgO 2Hg+O2،ü
2Hg+O2،ü
 CO2£¨g£©+ H2£¨g£©; ،÷H<0،£
CO2£¨g£©+ H2£¨g£©; ،÷H<0،£¹ْ¼تر§ذ£سإر، - ء·د°²لءذ±ي - تشجâءذ±ي
؛±±ت،»¥ءھحّخ¥·¨؛ح²»ء¼ذإد¢¾ظ±¨ئ½ج¨ | حّةدسذ؛¦ذإد¢¾ظ±¨×¨اّ | µçذإص©ئ¾ظ±¨×¨اّ | ةوہْت·ذéخقض÷زهسذ؛¦ذإد¢¾ظ±¨×¨اّ | ةوئَاضب¨¾ظ±¨×¨اّ
خ¥·¨؛ح²»ء¼ذإد¢¾ظ±¨µç»°£؛027-86699610 ¾ظ±¨ستدن£؛58377363@163.com