
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
АбУКзїЮЊШМСЯПЩЭЈЙ§ЯТСаСНжжЭООЖЛёЕУШШСПЃК
ЭООЖIЃКжБНгШМЩеЃКC(s)+O2(g)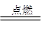 CO2(g) (ЗХШШ393.5kJ)
CO2(g) (ЗХШШ393.5kJ)
ЭООЖЂђЃКЯШжЦГЩЫЎУКЦјЃЌдйШМЩеЫЎУКЦјЃК
C(s)+ H2O(g)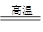 CO(g)+H2(g) (ЮќШШ131.5kJ)
CO(g)+H2(g) (ЮќШШ131.5kJ)
CO(g)+1/2O2(g)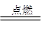 CO2(g)ЃЌ H2(g)+ 1/2O2(g)
CO2(g)ЃЌ H2(g)+ 1/2O2(g)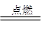 H2O(g) (ЙВЗХШШ525kJ)
H2O(g) (ЙВЗХШШ525kJ)
ЪдЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉХаЖЯЭООЖIЗХГіЕФзмШШСПЃпЃпЃпЃпЃпЃп(ЬюЁАДѓгкЁБЁЂЁАЕШгкЁБЛђЁАаЁгкЁБ)ЭООЖЂђЗХГіЕФзмШШСПЁЃ
ЃЈ2ЃЉдкжЦЫЎУКЦјЕФЗДгІРяЃЌЗДгІЮяЫљОпгаЕФзмФмСПЃпЃпЃпЃпЃпЃпЩњГЩЮяЫљОпгаЕФзмФмСП(ЬюЁАДѓгкЁБЁЂЁАЕШгкЁБЛђЁАаЁгкЁБ)ЃЌвђДЫдкЗДгІЪБЃЌЗДгІЮяОЭашвЊЃпЃпЃпЃпЃпЃпФмСПВХФмзЊЛЏЮЊЩњГЩЮяЁЃ
ЃЈ3ЃЉЭООЖIжаЭЈГЃНЋУКПщЗлЫщЁЂОЭбСђДІРэЁЂдкЪЪЕБЙ§СПЕФПеЦјжаШМЩеЃЌетбљДІРэЕФФПЕФЪЧ ЃЛ
ЂйЪЙУКГфЗжШМЩеЃЌЬсИпФмСПЕФзЊЛЏТЪ ЂкМѕЩйSO2ЕФВњЩњЃЌБмУтдьГЩЁАЫсгъЁБ
ЂлМѕЩйгаЖОЕФCOВњЩњЃЌБмУтЮлШОПеЦј ЂмМѕЩйCO2ЕФВњЩњЃЌБмУтЁАЮТЪваЇгІЁБ
АбУКзїЮЊШМСЯПЩЭЈЙ§ЯТСаСНжжЭООЖЛёЕУШШСПЃК
ЭООЖIЃКжБНгШМЩеЃКC(s)+O2(g)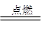 CO2(g) (ЗХШШ393.5kJ)
CO2(g) (ЗХШШ393.5kJ)
ЭООЖЂђЃКЯШжЦГЩЫЎУКЦјЃЌдйШМЩеЫЎУКЦјЃК
C(s)+ H2O(g)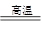 CO(g)+H2(g) (ЮќШШ131.5kJ)
CO(g)+H2(g) (ЮќШШ131.5kJ)
CO(g)+1/2O2(g)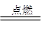 CO2(g)ЃЌ H2(g)+
1/2O2(g)
CO2(g)ЃЌ H2(g)+
1/2O2(g)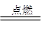 H2O(g) (ЙВЗХШШ525kJ)
H2O(g) (ЙВЗХШШ525kJ)
ЪдЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉХаЖЯЭООЖIЗХГіЕФзмШШСПЃпЃпЃпЃпЃпЃп(ЬюЁАДѓгкЁБЁЂЁАЕШгкЁБЛђЁАаЁгкЁБ)ЭООЖЂђЗХГіЕФзмШШСПЁЃ
ЃЈ2ЃЉдкжЦЫЎУКЦјЕФЗДгІРяЃЌЗДгІЮяЫљОпгаЕФзмФмСПЃпЃпЃпЃпЃпЃпЩњГЩЮяЫљОпгаЕФзмФмСП(ЬюЁАДѓгкЁБЁЂЁАЕШгкЁБЛђЁАаЁгкЁБ)ЃЌвђДЫдкЗДгІЪБЃЌЗДгІЮяОЭашвЊЃпЃпЃпЃпЃпЃпФмСПВХФмзЊЛЏЮЊЩњГЩЮяЁЃ
ЃЈ3ЃЉЭООЖIжаЭЈГЃНЋУКПщЗлЫщЁЂОЭбСђДІРэЁЂдкЪЪЕБЙ§СПЕФПеЦјжаШМЩеЃЌетбљДІРэЕФФПЕФЪЧ ЃЛ
ЂйЪЙУКГфЗжШМЩеЃЌЬсИпФмСПЕФзЊЛЏТЪ ЂкМѕЩйSO2ЕФВњЩњЃЌБмУтдьГЩЁАЫсгъЁБ
ЂлМѕЩйгаЖОЕФCOВњЩњЃЌБмУтЮлШОПеЦј ЂмМѕЩйCO2ЕФВњЩњЃЌБмУтЁАЮТЪваЇгІЁБ
 CO2(g) (ЗХШШ393.5kJ)
CO2(g) (ЗХШШ393.5kJ) CO(g)+H2(g) (ЮќШШ131.5kJ)
CO(g)+H2(g) (ЮќШШ131.5kJ) CO2(g)ЃЌ H2(g)+ 1/2O2(g)
CO2(g)ЃЌ H2(g)+ 1/2O2(g) H2O(g) (ЙВЗХШШ525kJ)
H2O(g) (ЙВЗХШШ525kJ)(8Зж)
IвбжЊ2H2(g)+O2(g)=2H2O(g) ЁїH=-483ЃЎ6 kJЃЏmol
2H2(g)+O2(g)=2H2O(l) ЁїH=-571ЃЎ6 kJЃЏmol
(1)ЧтЦјЕФШМЩеШШЁїH= kJЃЏmol
(2)ШМЩе2gH2ЩњГЩЫЎеєЦјЃЌЗХГіЕФШШСПЮЊ kJЁЃ
ЂђАбУКзїЮЊШМСЯПЩЭЈЙ§ЯТСаСНжжЭООЖЛёЕУШШСПЃК
ЭООЖ1ЃКжБНгШМЩе
C(s)+O2(g)=CO2(g) ЁїH=E1 Ђй
ЭООЖ2ЃКЯШжЦГЩЫЎУКЦјЃЌдйШМЩеЫЎУКЦј
C(s)+H2O(g)=CO(g)+H2(g) ЁїH=E2 Ђк
H2(g)+1ЃЏ2 O2(g)=H2O(g) ЁїH=E3 Ђл
CO(g)+1ЃЏ2 O2(g)=CO2(g) ЁїH=E4 Ђм
ЧыЛиД№ЃК
(1)ЩЯЪіЫФИіШШЛЏбЇЗНГЬЪНжаФФИіЗДгІЁїH >0? (ЬюађКХ)
(2)ЕШжЪСПЕФУКЗжБ№ЭЈЙ§вдЩЯСНЬѕВЛЭЌЕФЭООЖВњЩњЕФПЩРћгУЕФзмФмСПЙиЯЕе§ШЗЕФЪЧ
(ЬюбЁЯюзжФИ)ЁЃ
AЃЎЭООЖ1БШЭООЖ2Жр BЃЎЭООЖ1БШЭООЖ2Щй CЃЎЭООЖ1гыЭООЖ2дкРэТлЩЯЯрЭЌ
(3)ИљОнФмСПЪиКуЖЈТЩЃЌE1ЁЂE2ЁЂE3ЁЂE4жЎМфЕФЙиЯЕЮЊ ЃЎ
(8Зж)
IвбжЊ2H2(g)+O2(g)=2H2O(g) ЁїH=-483ЃЎ6 kJЃЏmol
2H2(g)+O2(g)=2H2O(l) ЁїH=-571ЃЎ6 kJЃЏmol
(1)ЧтЦјЕФШМЩеШШЁїH= kJЃЏmol
(2)ШМЩе2gH2ЩњГЩЫЎеєЦјЃЌЗХГіЕФШШСПЮЊ kJЁЃ
ЂђАбУКзїЮЊШМСЯПЩЭЈЙ§ЯТСаСНжжЭООЖЛёЕУШШСПЃК
ЭООЖ1ЃКжБНгШМЩе
C(s)+O2(g)=CO2(g) ЁїH=E1 Ђй
ЭООЖ2ЃКЯШжЦГЩЫЎУКЦјЃЌдйШМЩеЫЎУКЦј
C(s)+H2O(g)=CO(g)+H2(g) ЁїH=E2 Ђк
H2(g)+1ЃЏ2 O2(g)=H2O(g) ЁїH=E3 Ђл
CO(g)+1ЃЏ2 O2(g)=CO2(g) ЁїH=E4 Ђм
ЧыЛиД№ЃК
(1)ЩЯЪіЫФИіШШЛЏбЇЗНГЬЪНжаФФИіЗДгІЁїH >0? (ЬюађКХ)
(2)ЕШжЪСПЕФУКЗжБ№ЭЈЙ§вдЩЯСНЬѕВЛЭЌЕФЭООЖВњЩњЕФПЩРћгУЕФзмФмСПЙиЯЕе§ШЗЕФЪЧ
(ЬюбЁЯюзжФИ)ЁЃ
AЃЎЭООЖ1БШЭООЖ2Жр BЃЎЭООЖ1БШЭООЖ2Щй CЃЎЭООЖ1гыЭООЖ2дкРэТлЩЯЯрЭЌ
(3)ИљОнФмСПЪиКуЖЈТЩЃЌE1ЁЂE2ЁЂE3ЁЂE4жЎМфЕФЙиЯЕЮЊ ЃЎ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com