
题目列表(包括答案和解析)
1.《有机化学基础》
精神病学专家通过实验发现:在大脑的相应部位——“奖赏中心”,给予柔和的电击,便会处于似乎极度快乐的状态。人们已经将“奖赏中心”部分的脑电图绘制出来,并认为,在各区域之间传递信息的化学物质是多巴胺,所以“奖赏中心”又称为多巴胺系统。多巴胺结构如图。请回答下列问题:

(1)多巴胺的分子式:____________。
(2)试推测多巴胺能发生的反应类型____________。
A.消去 B.取代 C.加成 D.水解
(3)多巴胺可由香兰素与硝基甲烷制得,合成过程表示如下:

Ⅰ.0.5 mol香兰素发生银镜反应,最多可生成_________ mol Ag。
Ⅱ.②的结构简式是_________,生成②的反应类型是_________。
Ⅲ.写出④⑤步的化学方程式:
④_________________________________________________________________。
⑤_________________________________________________________________。
2.《物质结构与性质》下图是Na、Cu、Si、H、C、N等元素单质的熔点高低的顺序,其中c、d均是热和电的良导体。

(1)请写出图中b单质对应元素原子的电子排布式___________。
(2)单质a、f对应的元素以原子个数比1∶1形成的分子(相同条件下对H2的相对密度为13)中含___________个σ键和___________个π键。
(3)a与b的元素形成的10电子中性分子X的空间构型为___________;将X溶于水后的溶液滴入到AgNO3溶液中至过量,得到络离子的化学式为____________,其中X与Ag+之间以___________键结合。
(4)下图是上述六种元素中的一种元素形成的含氧酸的结构,请简要说明该物质易溶于水的原因____________________________________________________________________。

火力发电厂释放出大量的氮氧化物(NOx)、二氧化硫和二氧化碳等气体会造成环境污染。对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的。
(1)脱硝。利用甲烷催化还原NOx:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)
△H1=-574 kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)
△H2=-1160 kJ·mol-1
甲烷直接将NO2还原为N2的热化学方程式为__________。
(2)脱碳。将CO2转化为甲醇的热化学方程式为:
CO2(g)+3H2(g)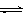 CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3
①取五份等体积CO2和H2的混合气体(物质的量之比均为1∶3),
分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间
后,测得甲醇的体积分数φ(CH3OH) 与反应温度T的关系曲线如下图所示,则
上述CO2转化为甲醇的反应的△H3__________0(填“>”、“<”或“=”)。
②在一恒温恒容密闭容器中充入1 mol CO2和3 mol H2,进行上述反应。测得CO2
和CH3OH(g)的浓度随时间变化如下图所示。下列说法正确的是__________(填
字母代号)。

A.第10 min后,向该容器中再充入1 mol CO2和3 mol H2,则再次达到平衡时c(CH3OH)=1.5 mol·L-1
B.0~10 min内,氢气的平均反应速率为0.075 mol/(L·min)
C.达到平衡时,氢气的转化率为0.75
D.该温度下,反应的平衡常数的值为3/16
E.升高温度将使n(CH3OH)/n(CO2)减小
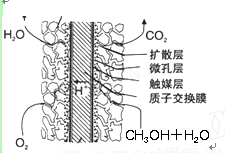
③甲醇燃料电池结构如下图所示。其工作时正极的电极反应式可表示为_______。
(3)脱硫。某种脱硫工艺中将废气经处理后,与一定量的氨气、空气反应,生成硫酸铵和硝酸铵的混合物作为副产品化肥。设烟气中的SO2、NO2的物质的量之比为1∶1,则该反应的化学方程式为__________。
(4)硫酸铵和硝酸铵的水溶液的pH<7,其中原因可用一个离子方程式表示为:__________;在一定物质的量浓度的硝酸铵溶液中滴加适量的NaOH溶液,使溶液的pH=7,则溶液中c(Na+)+c(H+)__________c(NO3-)+c(OH-)(填写“>”“=”或“<”)
火力发电厂释放出大量的氮氧化物(NOx)、二氧化硫和二氧化碳等气体会造成环境污染。对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的。
(1)脱硝。利用甲烷催化还原NOx:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574 kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H2=-1160 kJ·mol-1
甲烷直接将NO2还原为N2的热化学方程式为 。
(2)脱碳。将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H3
CH3OH(g)+H2O(g)△H3
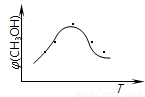
①取五份等体积CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH) 与反应温度T的关系曲线如下图所示,则上述CO2转化为甲醇的反应的△H3_______0(填“>”、“<”或“=”)。
②在一恒温恒容密闭容器中充入1 mol CO2和3 mol H2,进行上述反应。测得CO2和CH3OH(g)的浓度随时间变化如下图所示。下列说法正确的是__________(填字母代号)。
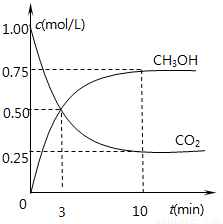
A.第10 min后,向该容器中再充入1 mol CO2和3 mol H2,则再次达到平衡时c(CH3OH)=1.5 mol·L-1
B.0-10 min内,氢气的平均反应速率为0.075 mol/(L·min)
C.达到平衡时,氢气的转化率为0.75
D.该温度下,反应的平衡常数的值为3/16
E.升高温度将使n(CH3OH)/n(CO2)减小
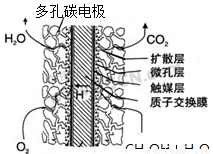
③甲醇燃料电池结构如下图所示。其工作时正极的电极反应式可表示为 。
(3)硫酸铵和硝酸铵的水溶液的pH<7,其中原因可用一个离子方程式表示为:__________;在一定物质的量浓度的硝酸铵溶液中滴加适量的NaOH溶液,使溶液的pH=7,则溶液中c(Na+)+c(H+)__________c(NO3-)+c(OH-)(填写“>”“=”或“<”)
火力发电厂释放出大量的氮氧化物(NOx)、二氧化硫和二氧化碳等气体会造成环境污染。对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的。
(1)脱硝。利用甲烷催化还原NOx:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)
△H1=-574 kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)
△H2=-1160 kJ·mol-1
甲烷直接将NO2还原为N2的热化学方程式为__________。
(2)脱碳。将CO2转化为甲醇的热化学方程式为:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3
①取五份等体积CO2和H2的混合气体(物质的量之比均为1∶3),
 分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间
分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间
后,测得甲醇的体积分数φ(CH3OH) 与反应温度T的关系曲线如下图所示,则
上述CO2转化为甲醇的反应的△H3__________0(填“>”、“<”或“=”)。

 ②在一恒温恒容密闭容器中充入1 mol CO2和3 mol H2,进行上述反应。测得CO2
②在一恒温恒容密闭容器中充入1 mol CO2和3 mol H2,进行上述反应。测得CO2
和CH3OH(g)的浓度随时间变化如下图所示。下列说法正确的是__________(填
字母代号)。
A.第10 min后,向该容器中再充入1 mol CO2和3 mol H2,则再次达到平衡时c(CH3OH)=1.5 mol·L-1
B.0~10 min内,氢气的平均反应速率为0.075 mol/(L·min)
C.达到平衡时,氢气的转化率为0.75
D.该温度下,反应的平衡常数的值为3/16
E.升高温度将使n(CH3OH)/n(CO2)减小
③甲醇燃料电池结构如下图所示。其工作时正极的电极反应式可表示为_______。

多孔碳电极
(3)脱硫。某种脱硫工艺中将废气经处理后,与一定量的氨气、空气反应,生成硫酸铵和硝酸铵的混合物作为副产品化肥。设烟气中的SO2、NO2的物质的量之比为1∶1,则该反应的化学方程式为__________。
(4)硫酸铵和硝酸铵的水溶液的pH<7,其中原因可用一个离子方程式表示为:__________;在一定物质的量浓度的硝酸铵溶液中滴加适量的NaOH溶液,使溶液的pH=7,则溶液中c(Na+)+c(H+)__________c(NO3-)+c(OH-)(填写“>”“=”或“<”)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com