
题目列表(包括答案和解析)
在密度为1.16g/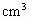 的浓盐酸A中,含有31.5%的HCl,则10mLA中溶有________g
HCl. 在50mL A中加水至溶液为1L时,得到________mol/L的盐酸B,从中取出10mL,其物质的量浓度为________mol/L.如果将1.0g的NaOH、KOH的混合物溶于水,用B来中和,需46mL B,可知1.0g碱的混合物中含有________g NaOH,NaOH与KOH的物质的量之比是________.
的浓盐酸A中,含有31.5%的HCl,则10mLA中溶有________g
HCl. 在50mL A中加水至溶液为1L时,得到________mol/L的盐酸B,从中取出10mL,其物质的量浓度为________mol/L.如果将1.0g的NaOH、KOH的混合物溶于水,用B来中和,需46mL B,可知1.0g碱的混合物中含有________g NaOH,NaOH与KOH的物质的量之比是________.
(15分)氯化铁是常见的水处理剂,无水氯化铁的熔点为555K、沸点为588K。工业制备氯化铁的一种工艺如下:
回答下列问题
(1)取0.5mL氯化铁溶液滴入50mL沸水中,再煮沸片刻得红褐色透明液体,该过程可用离子方程式表示为 。
(2)已知FeCl3·6H2O在水中的溶解度如下:
| 温度/℃ | 0 | 10 | 20 | 30 | 50 | 80 | 100 |
| 溶解度(g/100gH2O) | 74.4 | 81.9 | 91.8 | 106.8 | 315.1 | 525.8 | 535.7 |
从FeCl3溶液中获得FeCl3·6H2O的方法是 。
(3)捕集器中温度超过673K,存在相对分子质量为325的物质,该物质的化学式为 。
(4)室温时向FeCl3溶液中滴加NaOH溶液,当溶液中c(Fe3+)≤1.0×10-5 mol·L-1时,视作Fe3+沉淀完全,则Fe3+沉淀完全的pH至少为 (已知Ksp[Fe(OH)3]=1.0×10-38)。
(5)吸收剂X是 ,吸收塔中吸收剂X的作用是 。
(6)测定样品中FeCl3的质量分数的方法是:
a.称取mg无水氯化铁样品,溶于稀盐酸,再转移到100mL容量瓶,用蒸馏水定容
b.取出10mL待测溶液于锥形瓶中,加入稍过量的KI溶液充分反应
c.以淀粉作指示剂,用b mol·L-1Na2S2O3溶液滴定(I2+2 Na2S2O3=Na2S4O6+2NaI),共用去VmL。①样品中氯化铁的质量分数为 。
②若用上述办法测定的样品中FeCl3的质量分数偏低(测定过程中产生的误差可忽略),其原因可能是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com