
̀âÄ¿Áбí(°üÀ¨´đ°¸ºÍ½âÎö)
 ʵÑéỂĐèÓĂ98 ml 1.0 mol/L Ạ́ËᣬÏÖÓĂŨẠ́Ëᣨ±êÇ©ÈçÏÂͼ£©ÅäÖÆ¡£ÊµÑé̉ÇÆ÷ÓĐ£ºA£®25 mlÁ¿Í² B£®ÍĐÅ̀̀́ƽ C£®²£Á§°ô D£®50 mlÈƯÁ¿Æ¿ E£®10 mlÁ¿Í² F£®½ºÍ·µÎ¹Ü G£®50 mlÉƠ± H£®100 mlÈƯÁ¿Æ¿ I£®200 mlÈƯÁ¿Æ¿
ʵÑéỂĐèÓĂ98 ml 1.0 mol/L Ạ́ËᣬÏÖÓĂŨẠ́Ëᣨ±êÇ©ÈçÏÂͼ£©ÅäÖÆ¡£ÊµÑé̉ÇÆ÷ÓĐ£ºA£®25 mlÁ¿Í² B£®ÍĐÅ̀̀́ƽ C£®²£Á§°ô D£®50 mlÈƯÁ¿Æ¿ E£®10 mlÁ¿Í² F£®½ºÍ·µÎ¹Ü G£®50 mlÉƠ± H£®100 mlÈƯÁ¿Æ¿ I£®200 mlÈƯÁ¿Æ¿
£¨1£©ÊµÑéʱӦѡÓõÄ̉ÇÆ÷ÊÇ£῭îÈë±àºÅ£©_________¡£
£¨2£©ËùĐèŨẠ́ËáµÄ̀å»ưÊÇ________ml¡£
£¨3£©ÏÂÁĐ´íÎó²Ù×÷¿ÉʹËùÅäÖÆÈÜ̉ºÅ¨¶ÈÆ«¸ßµÄÊÇ
A£®ÈƯÁ¿Æ¿Ï´µÓºóδ¸ÉÔï
B£®Èܽâ½Á°èʱÓĐ̉º̀å·É½¦
C£®¶¨ÈƯʱ¸©ÊÓÈƯÁ¿Æ¿Æ¿¾±¿̀¶ÈÏß
D£®̉¡ÔȺó¼û̉ºĂæϽµ£¬ÔÙ¼ÓË®ÖÁ¿̀¶ÈÏß
Ó̉ͼΪʵÑéỂijŨẠ́ËáËáÊÔ¼ÁÆ¿±êÇ©ÉϵÄÓĐ¹ØÊư¾Ư£¬
|
£¨1£©¸ĂŨẠ́ËáµÄÎïÖʵÄÁ¿Å¨¶ÈΪ ¡£
£¨2£©Ê¹ÓĂÈƯÁ¿Æ¿Ç°±ØĐë½øĐеÄ̉»²½²Ù×÷ÊÇ___________
£¨3£©Ä³Ñ§ÉúÓûÓĂÉÏÊöŨẠ́ËáºÍƠôÁóË®ÅäÖÆ500 ml ÎïÖʵÄÁ¿
Ũ¶ÈΪ1.0 mol¡¤L-1Ï¡Ạ́Ëá¡£
¢Ù¸ĂѧÉúĐè̉ªÁ¿È¡ ml ÉÏÊöŨẠ́Ëá½øĐĐÅäÖÆ¡£
¢ÚÈƯÁ¿Æ¿ÉÏĐè±êÓĐ̉ÔÏÂÎåÏîÖеÄ
AÎÂ¶È BŨ¶È CÈƯÁ¿ Dѹǿ E¿̀¶ÈÏß
¢ÛÔÚÅäÖƹư³̀ÖĐ£¬ÏÂÁĐʵÑé²Ù×÷¶ÔËùÅäÖƵÄÏ¡Ạ́ËáµÄÎïÖʵÄÁ¿Å¨¶ÈÓĐºÎÓ°Ḯ£¿
£¨ÔÚºóĂæºáÏßÉÏ¡°Æ«¸ß¡±¡¢¡°Æ«µÍ¡±¡¢¡°Î̃Ó°Ḯ¡±£©¡£
I¡¢ÓĂÁ¿Í²Á¿È¡Å¨Ạ́Ëáʱ¸©ÊÓ°¼̉ºĂæ¡¡¡¡¡¡¡¡
II¡¢¶¨ÈƯºó¾Ơñµ´¡¢̉¡ÔÈ¡¢¾²ÖĂ£¬·¢ÏÖ̉ºĂæϽµ£¬ÔÙ¼ÓÊÊÁ¿µÄƠôÁóË®¡¡¡¡¡¡¡¡¡¡¡¡
¢ó¡¢¶¨ÈƯʱÑöÊÓÊÓ¿̀¶ÈÏß
¢ô¡¢×ª̉ÆʱÈƯÁ¿Æ¿ÖĐÓĐÉÙÁ¿ƠôÁóË®
ÓûÓĂÖÊÁ¿·ÖÊưΪ98£¥µÄŨẠ́Ëá(¦Ñ£½1.84 g/cm3)ÅäÖƳÉŨ¶ÈΪ0.5 mol/LµÄÏ¡Ạ́Ëá500 mL£®
(1)Ñ¡ÓõÄÖ÷̉ª̉ÇÆ÷ÓĐ________£®
(2)Ç뽫ÏÂÁи÷²Ù×÷£¬°´ƠưÈ·µÄĐ̣ºÅ̀îÔÚºáÏßÉÏ£®
A£®ÓĂÁ¿Í²Á¿È¡̉»¶῭å»ưµÄŨH2SO4
B£®·´¸´µßµ¹̉¡ÔÈ
C£®¼ÓƠôÁóË®ÖÁ¾à¿̀¶È2¡«3 cmʱ£¬¸ÄÓĂ½ºÍ·µÎ¹Ü¼ÓË®ÖÁ¿̀¶È
D£®ÓĂÉÙÁ¿ƠôÁóˮϴµÓÉƠ±ºÍ²£Á§°ô2¡«3´Î£¬²¢½«Ï´µÓ̉º̉»²¢×ª̉ÆÖÁÈƯÁ¿Æ¿£¬̉¡ÔÈ
E£®ÔÚÉƠ±ÖĐÏ¡ÊÍŨH2SO4
F£®¾²ÖĂ£¬´ưÈÜ̉º»Ö¸´ÖÁỂκ󣬽«ÈÜ̉º×ªÈëÈƯÁ¿Æ¿
G£®½«ËùÅäÈÜ̉º×ª̉ÆÖÁ½à¾»¸ÉÔïµÄÊÔ¼ÁÆ¿£¬²¢̀ùÉϱêÇ©
Æä²Ù×÷ƠưÈ·µÄ˳Đ̣̉À´ÎΪ________£®
(3)¼̣̉ª»Ø´đÏÂÁĐÎỀ⣺
¢ÙËùĐèŨẠ́ËáµÄ̀å»ưΪ________mL£®
¢ÚÈç¹ûʵÑéỂÓĐ15 mL¡¢20 mL¡¢50 mLµÄÁ¿Í²Ó¦Ñ¡ÓĂ________mLµÄÁ¿Í²×îºĂ£¬Á¿È¡Ê±·¢ÏÖÁ¿Í²²»¸É¾»ÓĂˮϴ¾»ºóÖ±½ÓÁ¿È¡»áʹŨ¶È________£®
¢Û½«Å¨Ạ́ËáÑØÉƠ±ÄÚ±ÚÂưÂư×¢ÈëʢˮµÄÉƠ±ÖĐ£¬²¢²»¶Ï½Á°èµÄÄ¿µÄÊÇ________£¬Èô½Á°è¹ư³̀ÖĐÓĐ̉º̀彦³ö»áʹŨ¶ÈÆ«________£®
¢ÜÔÚתÈëÈƯÁ¿Æ¿Ç°ÉƠ±ÖĐ̉º̀åÓ¦________£¬·ñỘ»áʹŨ¶È________£»²¢Ï´µÓÉƠ±2¡«3´Î£¬Ï´µÓ̉º̉²̉ª×ªÈëÈƯÁ¿Æ¿£¬·ñỘ»áʹŨ¶È________£®
¢Ư¶¨ÈƯʱ±ØĐëʹÈÜ̉º°¼̉ºĂæÓë¿̀¶ÈÏàƽ£¬Èô¸©ÊÓ½á¹û»áʹŨ¶È________£»ÑöÊÓỘʹŨ¶È________£®
£¨08³¤É³ÑÅÀñÖĐѧ̉»Ä££©£¨16·Ö£©Ä³¿ÎÍâʵÑéĐ¡×éѧÉúÀûÓĂÏÂͼËùʾװÖĂ½øĐĐ¡°̉̉¶₫ËᣨË×Ăû²ƯËᣩ¾§̀åÊÜÈȷֽ⡱µÄʵÑ飬²¢ÑéÖ¤·Ö½â²úÎïÖĐÓĐCO2ºÍCO¡££¨Í¼ÖĐ¼Đ³Ö×°ÖẲÑÂÔÈ¥£©
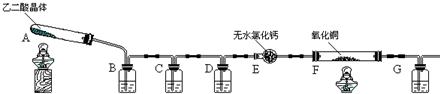 |
£¨1£©×°ÖĂCÖĐÊ¢·Å ÈÜ̉º£»DµÄ×÷ÓĂÊÇ £»
£¨2£©Ö¤Ă÷·Ö½â²úÎïÖĐÓĐCOµÄÏÖÏóÊÇ £»
£¨3£©¸Ă×°ÖĂÓĐ̉»¸ö²»×ăÖ®´¦£¬ÇëĐ´³ö £»
£¨4£©Ä³Í¬Ñ§²éÔÄÏà¹Ø×ÊÁÏ£º²ƯËáÊǶ₫ÔªËᣬËáĐÔ±È̀¼ËáÇ¿£¬ÔÚÊÜÈÈ·Ö½â¹ư³̀ÖĐÓĐÉÙÁ¿Éư»ª£»²ƯËá¸ÆºÍ²ƯËáÇâ¸Æ¾ùΪ°×É«²»ÈÜÎï¡£̣̉´Ë¸ĂͬѧÈÏΪ£ºĐè̉ªÔÚ×°ÖĂB֮ǰÔö¼Ó̉»¸ö×°ÓĐ________£῭îĐ´ÏÂÁбàºÅ×Öĸ£©µÄÏ´Æø×°ÖĂ¡£
a£®Ë® b£®NaOH ÈÜ̉º c£®Na2CO3 ÈÜ̉º d£®±¥ºÍNaHCO3 ÈÜ̉º
£¨5£©²ƯËá¿É̉ÔÔÚËáĐỒơ¼₫ϱ»KMnO4Ñơ»¯£¬·´Ó¦µÄÀë×Ó·½³̀ʽΪ£º
2MnO4£ + 5H2C2O4 +6 H+ = 2Mn2+ +10 CO2¡ü+8 H2O
ʵÑéỂ³£ÓĂ²ƯËáÄƱ궨KMnO4ÈÜ̉º¡£²Ù×÷ÈçÏ£º×¼È·³ÆÈ¡2.680 g²ƯËáÄÆ£¬·ÅÈë׶ĐÎÆ¿ÖĐ£¬¼Ó100 mLÏ¡Ạ́ËáÈܽ⣬½«×¶ĐÎÆ¿ÖĂÓÚ £῭î¡°Ëáʽ¡± ¡°¼îʽ¡±£©µÎ¶¨¹ÜÏ£¬ÓĂKMnO4ÈÜ̉ºµÎ¶¨¡£µ± ʱ£¬¼´´ïµ½µÎ¶¨ÖƠµă¡£Öظ´ÉÏÊöµÎ¶¨²Ù×÷Èư´Î£¬ÊµÑéÊư¾ƯÈçϱíËùʾ¡£
| µÎ¶¨Ç° | µÚ̉»´ÎÖƠµă | µÚ¶₫´ÎÖƠµă | µÚÈư´ÎÖƠµă | µÚËÄ´ÎÖƠµă |
µÎ¶¨¹Ü ̉ºĂæ¿̀¶È | 0.00 mL | 20.02 mL | 21.00mL | 19.98 mL | 20.00mL |
KMnO4ÈÜ̉ºµÄÎïÖʵÄÁ¿Å¨¶ÈµÄÊÇc(KMnO4)= mol?L£1¡£
£¨12·Ö£©£¨1£©ÏÂÁĐĂ¿×éÖж¼ÓĐ̉»ÖÖÎïÖÊÓëÆäËûÎïÖÊÔÚ·ÖÀàÉϲ»Í¬£¬ÊÔ·ÖÎöĂ¿×éÖĐÎïÖʵÄ×é³É¹æÂÉ£¬½«ƠâÖÖ²»Í¬ÓÚÆäËûÎïÖʵÄÎïÖÊỞ³öÀ´£®
¢ÙNaCl¡¢KCl¡¢NaClO¡¢BaCl2 ¢Ú×Ç̉º¡¢ÈÜ̉º¡¢½º̀塢ˮ
£¨2£©ÓĂ98%µÄŨH2SO4(¦Ñ£½1.84 g/cm3)ÅäÖÆ500 ml¡¡0.5 mol/LµÄÏ¡H2SO4£¬ËùĐèŨH2SO4µÄ̀å»ưΪ________ml£¨Đ¡Êưµăºó±£Áổ»Î»ÓĐЧÊư×Ö£©£¬Èç¹ûʵÑéỂÓĐ10 ml¡¢20 ml¡¢50 mlÁ¿Í²£¬Ó¦Ñ¡ÓĂ mlÁ¿Í²£¬ÊµÑéÖĐ»¹Đè̉ªÓõ½µÄ̉ÇÆ÷ÓĐ £¬ÈôʵÑéÖĐ³öÏÖÏÂÁĐÏÖÏó¶ÔËùÅäÈÜ̉ºÅ¨¶ÈÓĐÊ²Ă´Ó°Ḯ£¿(̀îÆ«¸ß¡¢Æ«µÍ¡¢Î̃Ó°Ḯ)
¢ÙŨẠ́ËáÈܽâºóδÀäÈ´ÖÁỂμ´×ª̉ÆÖÁÈƯÁ¿Æ¿½øĐж¨ÈƯ________¢Ú¶¨ÈƯʱÑöÊÓ¿̀¶ÈÏß
¢ÛÁ¿È¡ºĂŨẠ́Ëáµ¹ÈëÉƠ±Èܽâºó£¬ÓĂˮϴµÓÁ¿Í²2-3´Î£¬½«Ï´µÓ̉ºµ¹ÈëÉƠ±
£¨3£©7.8gµÄĂ¾ÂÁºÏ½đÓë×ăÁ¿µÄÏ¡ÑÎËá·´Ó¦£¬Éú³ÉÇâÆøµÄ̀å»ưΪ8.96L£¨±ê×¼×´¿ö£©£¬Ộ´Ë·´Ó¦ÖĐת̉Ƶç×ӵĸöÊưΪ________________£¬ÓÉĂ¾ºÍÂÁ·Ö±đ²úÉúµÄÇâÆøµÄ̀å»ưÖ®±ÈΪ________________
£¨4£©È¡100mlµÄNa2CO3ºÍNa2SO4µÄ»́ºÏÈÜ̉ºÓë¹ưÁ¿ÑÎËá·´Ó¦£¬Éú³É0.896L£¨±ê¿ö£©CO2£»ÈôỊ̈Ô»́ºÏÈÜ̉ºÖĐ¼ÓÈë×ăÁ¿µÄBa(OH)2ÈÜ̉º£¬µĂµ½³ÁµíµÄÖÊÁ¿Îª10.21g£¬ÊÔ¼ÆËă»́ºÏÈÜ̉ºÖĐNa2CO3µÄÎïÖʵÄÁ¿Å¨¶ÈÊÇ___________mol/L, Na2SO4µÄÎïÖʵÄÁ¿Å¨¶ÈÊÇ___________mol/L¡£
¹ú¼ÊÑ§Đ£ÓÅÑ¡ - Á·Ï°²áÁбí - ÊỒâÁбí
º₫±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨Æ½̀¨ | ÍøÉÏÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | µçĐÅƠ©Æ¾Ù±¨×¨Çø | ÉæÀúÊ·ĐéÎ̃Ö÷̉åÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com