2010年7月19~28日,第42届国际奥林匹克化学竞赛在日本东京举行,来自70多个国家和地区的280名中学生选手参加了本次竞赛.我国选派的四名选手全部获得金牌.中国国家代表队是此次比赛中唯一一支四名选手均获金牌的队伍,总分位列第一.请你回答以下问题:
(1)下列说法中不正确的是
.
A.三氧化二铝属于碱性氧化物
B.用热的纯碱溶液洗涤沾有油污的物品时,发生的主要是化学变化
C.光导纤维的基本原料为SiO
2D.液氨、液氯、液态氯化氢都是非电解质
E.丁达尔效应可用于区别溶液与胶体,云、雾均能产生丁达尔效应
(2)人们对酸碱的认识,已有几百年的历史,经历了一个由浅入深,由低级到高级的认识过程.
①1887年阿仑尼乌斯提出电离理论.
②1923年丹麦化学家布朗斯特和英国化学家劳莱提出了质子论.凡是能够释放质子(氢离子)的任何含氢原子的分子或离子都是酸;凡是能与质子(氢离子)结合的分子或离子都是碱.按质子理论:下列粒子的水溶液既可看作酸又可看作碱的是
.
A.H
2O B.NH
4+C.OH
-D.HCO
3-E.CH
3COO
-F.Cl
-③1923年路易斯(Lewis)提出了广义的酸碱概念.凡是能给出电子对而用来形成化学键的物质是碱;凡是能和电子对结合的物质都是酸.
如:酸(电子对接受体)碱(电子对给予体)反应产物H
++[:OH]
-→H:OH
试指出下列两个反应中的酸或碱:
H
3BO
3+H
2O═H
++[B(OH)
4]
-;该反应中的碱是
(填“H
3BO
3”或“H
2O”).
CuCl
2+4NH
3═[Cu (NH
3)
4]
2++2Cl
-;该反应中的酸是
(填“CuCl
2”或“NH
3”).



 ,俗名为水杨酸,在医学上具有 作用
,俗名为水杨酸,在医学上具有 作用 

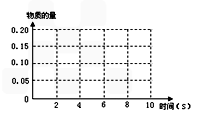
 2CO2(g)+N2(g) 在某温度T1℃下,2L密闭容器中充入NO 、CO各0.4mol,测得不同时间的NO和CO物质的量如下表:
2CO2(g)+N2(g) 在某温度T1℃下,2L密闭容器中充入NO 、CO各0.4mol,测得不同时间的NO和CO物质的量如下表: