
题目列表(包括答案和解析)
某同学准备用CuSO4·5H2O配制480 mL 1 mol/L的溶液.
(1)该同学选用的容量瓶容积的规格是________mL;
(2)玻璃棒在该实验中有重要的用途,分别是________和________;
(3)配制好的溶液呈________色.该同学还想通过实验分别证实溶质中含有Cu2+、SO42-,请你帮他想想办法,选择适当的试剂(写化学式),并写出其相应的离子方程式.

(4)物质的量浓度误差分析:(填偏高、偏低、无影响)
①若容量瓶洗净后未干燥,残留少量水,则所配制的溶液浓度将________;
②定容时,若眼睛俯视,则所配制的溶液浓度将________.
某兴趣小组设计并进行了以下实验来探究Cl2、漂白粉的制备及有关性质。
(1)实验室拟用下列装置制备干燥纯净的氯气,请按照气体从左向右流动的方向将仪器进行连接:
H→ 、 → 、 → ;广口瓶Ⅱ中的试剂为 。

(2)写出工业上用氯气和石灰乳制取漂白粉的化学反应方程式:
;
某学生设计如下实验进一步探究SO2与漂粉精的反应:
|
操作 |
现象 |
|
取4 g漂粉精固体,加入100 mL水 |
部分固体溶解,溶液略有颜色 |
|
过滤,测漂粉精溶液的pH |
pH试纸先变蓝(约为12),后褪色 |
|
A |
ⅰ.液面上方出现雾状物 ⅱ.稍后,出现浑浊,溶液变为黄绿色 ⅲ.稍后,产生大量白色沉淀,黄绿色褪去 |
(3)pH试纸颜色的变化说明漂粉精溶液具有的性质是 。
(4)该同学推测现象i的雾状物由盐酸小液滴形成,进行如下实验加以进一步验证:
a.用湿润的碘化钾淀粉试纸检验雾状物,无变化;
b.搜集雾状物,用酸化的AgNO3溶液检验,产生白色沉淀。
实验a的目的是 。
(5)现象ⅱ中溶液变为黄绿色的可能原因:随溶液酸性的增强,漂粉精的某些成份之间发生反应。请设计实验方案,进一步确认这种可能性,方案为
。
(6)用化学方程式解释现象ⅲ中黄绿色褪去的原因: 。检验褪色后溶液中是否有 的方法是:
。
的方法是:
。
(1)常温下,高锰酸钾晶体遇浓盐酸会生成一种气体,该气体是由瑞典化学家舍勒首先发现的。如图所示,将浓盐酸小心滴入Y形管B端。
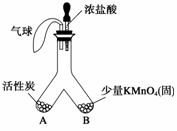
①开始观察到的现象是 。
②一段时间后又可观察到 ,请解释这一现象 。
③应用活性炭的此性质可制作 来达到防毒、防臭的目的(举一例即可)。
(2)①写出CO2和Na2O2反应的化学方程式 。
②某学生判断SO2和Na2O2反应能生成硫酸钠,你认为他的判断合理吗? 。
简要说明理由: 。
③该同学无法断定反应中是否有氧气生成,拟使用如图所示装置进行实验(图中铁架台等装置已略去)。
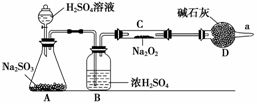
装置中B的作用是 ,
D的作用是 。
④如何证明该同学的两个推断?
。
某校课外兴趣小组用如图装置进行电解CuC12溶液的实验。实验时,在通电一段时间后,观察到阳极上方的淀粉KI试纸不变色,同时,铁棒逐渐溶解;阴极碳棒上有红、白两种颜色的固体析出。同学们对阴、阳两极的产物进行如下探究:
 (1)阳极产物探究。
(1)阳极产物探究。
根据实验现象,同学们对阳极发生的电极反应提出了如下假设:
假设1 Fe-3e == Fe3+ ;
假设2 。
请你设计实验方案证明你的假设(包括:操作→现象→结论)
(2)阴极产物探究:
| 查阅资料 | 铜和铜的化合物中Cu、Cu2O为红色,CuCl、CuBr、CuI为白色,它们在水中均不溶,且稳定存在。 |
| 探究实验 | 取出阴极碳棒,并将其干燥,然后用如图所示装置(气密性良好,药品性能良好)进行实验并记录现象: 现象:碳棒上红色物质依然存在;白色物质变为红色;无水硫酸铜仍为白色;蓝色石蕊试纸变为红色 |
结论与解释:
①白色物质为 。
②某学生收集碳棒上的白色物质并装入试管中,滴人稀HNO3,写出白色物质与稀HNO3反应的离子方程式: 。(不需要配平)

用实验室制氧气(以氯酸钾为原料,二氧化锰作催化剂)的残渣为原料,制备氯化氢气体.
(1)某学生提出的实验步骤依次是:溶解、蒸发、结晶、制取气体.其中还缺少的必要步骤是( )
(2)某学生开列的实验用品为:烧杯、圆底烧瓶、蒸发皿、量筒、集气瓶、分液漏斗、酒精灯、药匙、托盘天平、铁架台、铁夹、铁圈、双孔橡皮塞、玻璃导管、橡皮管、火柴、蒸馏水.
所缺少的必要试剂是________,所缺少的必要的实验用品是(错答要倒扣分)________.
(3)写出本实验中制取氯化氢气体的化学方程式________.
(4)本实验吸收尾气的装置所用的仪器是________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com