
题目列表(包括答案和解析)
(16分)碳及其化合物与人类生产、生活密切相关。请回答下列问题:
(1)在化工生产过程中,少量CO的存在会引起催化剂中毒。为了防止催化剂中毒,常用SO2将CO氧化SO2被还原为S。
已知: C(s)+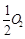 (g)=CO(g)ΔH1=-126.4kJ/mol ①
(g)=CO(g)ΔH1=-126.4kJ/mol ①
C(s)+O2(g)=CO2(g) ΔH2= -393.5kJ·mol-1 ②
S(s)+O2(g)=SO2(g) ΔH3= -296.8kJ·mol-1 ③
则SO2氧化CO的热化学反应方程式:
(2)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g) CH3OH(g)。
CH3OH(g)。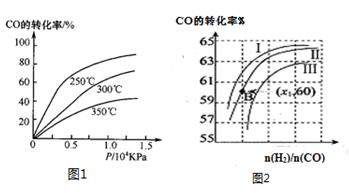
①CO在不同温度下的平衡转化率与压强的关系如图1所示,该反应ΔH 0(填“>”或“ <”)。
图2表示CO的转化率与起始投料比[ n(H2)/n(CO)]、温度的变化关系,曲线I、II、III对应的平衡常数分别为K1、K2、K3,则K1、K2、K3的大小关系为 ;测得B(X1,60)点氢气的转化率为40%,则x1= 。
②在恒容密闭容器里按体积比为1:2充入一氧化碳和氢气,一定条件下反应达到平衡状态。当改变反应的某一个条件后,下列变化能说明平衡一定向正反应方向移动的是 (填序号)。
| A.正反应速率先增大后减小 | B.逆反应速率先增大后减小 |
| C.化学平衡常数K值增大 | D.反应物的体积百分含量增大 |
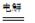 CH3CHOH+CH3CHOOH。
CH3CHOH+CH3CHOOH。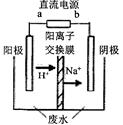
 (g)=CO(g)ΔH1=-126.4kJ/mol ①
(g)=CO(g)ΔH1=-126.4kJ/mol ① CH3OH(g)。
CH3OH(g)。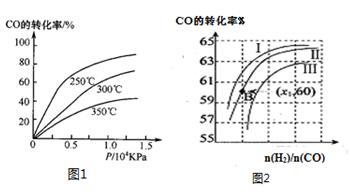
| A.正反应速率先增大后减小 | B.逆反应速率先增大后减小 |
| C.化学平衡常数K值增大 | D.反应物的体积百分含量增大 |
 CH3CHOH+CH3CHOOH。
CH3CHOH+CH3CHOOH。
(9分)NO分子因污染空气而臭名昭著。近年来,发现少量的NO在生物体内许多组织中存在,它有扩张血管、免疫、增强记忆的功能,而成为当前生命科学的研究热点,NO亦被称为“明星分子”。
请回答下列问题。
(1)对NO的叙述正确的是________(填序号)。
A.NO是一种无色有毒的气体 B.常温、常压下,NO难与空气中的O2化合
C.含等质量氧元素的NO和CO的物质的量相等 D.NO易溶于水,不能用排水法收集
(2)NO对环境的危害在于________(填序号)。
A.破坏臭氧层 B.高温下能使一些金属被氧化 C.造成酸雨 D.与人体血红蛋白结合
(3)在含Cu+的酶的活化中心中,亚硝酸根离子可转化为NO。写出Cu+和亚硝酸根离子在酸性水溶液中反应的离子方程式为:_________________________________________。
(4)在常温下,把NO气体压缩到100个大气压,在一个体积固定的容器里加热到50℃,发现气体的压力迅速下降,压力降至略小于原压力的2/3就不再改变,已知其中一种产物为N2O,写出上述变化的化学方程式:___________________________________________。
(5)解释变化(4)中为什么最后的气体总压力小于原压力的2/3?
________________________________________________________________________
________________________________________________________________________。
(9分)NO分子因污染空气而臭名昭著。近年来,发现少量的NO在生物体内许多组织中存在,它有扩张血管、免疫、增强记忆的功能,而成为当前生命科学的研究热点,NO亦被称为“明星分子”。
请回答下列问题。
(1)对NO的叙述正确的是________(填序号)。
A.NO是一种无色有毒的气体 B.常温、常压下,NO难与空气中的O2化合
C.含等质量氧元素的NO和CO的物质的量相等 D.NO易溶于水,不能用排水法收集
(2)NO对环境的危害在于________(填序号)。
A.破坏臭氧层 B.高温下能使一些金属被氧化 C.造成酸雨 D.与人体血红蛋白结合
(3)在含Cu+的酶的活化中心中,亚硝酸根离子可转化为NO。写出Cu+和亚硝酸根离子在酸性水溶液中反应的离子方程式为:_________________________________________。
(4)在常温下,把NO气体压缩到100个大气压,在一个体积固定的容器里加热到50℃,发现气体的压力迅速下降,压力降至略小于原压力的2/3就不再改变,已知其中一种产物为N2O,写出上述变化的化学方程式:___________________________________________。
(5)解释变化(4)中为什么最后的气体总压力小于原压力的2/3?
________________________________________________________________________
________________________________________________________________________。
某学生将H2O2溶液滴入含有酚酞的NaOH溶液中,观察到溶液的红色消失.为了探究溶液褪色的原因,该同学查阅了资料:“过氧化氢(H2O2)是一种无色粘稠液体,有较强的氧化性,它的水溶液俗称双氧水,呈弱酸性.过氧化氢贮存时会分解为水和氧气.如在它的水溶液中加入少量二氧化锰,可以极大地促进它的分解.因此实验室里常用过氧化氢来制取氧气.”据此,该同学对溶液褪色的原因作出了两种假设,然后他又通过设计一个简单的实验,对这两种假设作了验证,证实有一种假设可能是错误的.
请回答:
(1)该同学作出的两种假设是什么?________
(2)该同学设计了一个什么实验来证实其中一种假设可能是错误的?(说出该实验的方法及根据哪些现象作出判断)________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com